
现有甲、乙、丙三种晶体的晶胞(甲中X处于晶胞的中心,乙中A处于晶胞的中心),可推知,甲晶体中X与Y的个数比是________,乙中A与B的个数比是________,丙晶胞中有________个C离子,有________个D离子。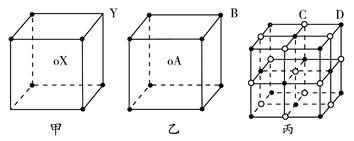
科目:高中化学 来源: 题型:单选题
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞。若再将在成键的C原子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞。则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)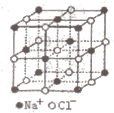
| A.一个金刚石的晶胞中有8个C原子 |
| B.金刚石的密度为3.54g·cm-1 |
| C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D.在该种CO2晶胞中含氧原子8个 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
原子晶体干冰具有类似SiO2的晶体结构,下列有关它的推断中,错误的是
| A.它可作耐磨材料 |
| B.它不可用作致冷剂 |
| C.晶体中每个碳原子形成2个碳氧双键 |
| D.晶体中碳、氧原子个数之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(8分)选择以下物质填写下列空白:
| A.氢氧化钠 | B.氧化镁 | C.He | D.二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)下图是石墨的结构,其晶体中存在的作用力有 (填序号) 
A:σ键 B:π键 C:氢键 D:配位键 E:分子间作用力 F:金属键 G:离子键
(2) 下面关于晶体的说法不正确的是___________
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由高到低:Na>Mg>Al |
| D.晶格能由大到小:NaF> NaCl> NaBr>NaI |


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知尿素的结构式为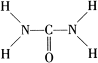 : 尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
: 尿素可用于制有机铁肥,主要代表物有三硝酸六尿素合铁(Ⅲ),化学式为[Fe(H2NCONH2)6](NO3)3。
(1)基态Fe3+的核外电子排布式为 ;C、N、O三种元素的第一电离能由大到小的顺序是 。
(2)尿素分子中N原子的杂化方式是 。
(3)NH+4中H—N—H键角比NH3中H—N—H键角大,原因为 。
(4)CO2和NH3是工业上制备尿素的重要原料,固态CO2(干冰)的晶胞结构如右图所示。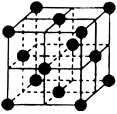
①1个CO2分子周围等距离且距离最近的CO2分子有 个。
②NaCl晶胞也为面心立方结构,已知NaCl晶体密度为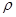 g·cm-3,NA表示阿伏加德罗常数,则NaCl晶胞体积为 cm3
g·cm-3,NA表示阿伏加德罗常数,则NaCl晶胞体积为 cm3
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硼元素B在化学中有很重要的地位。硼的化合物在农业、医药、玻璃等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式_________________。从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为___________。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是_____________________________。
(3)在BF3分子中中心原子的杂化轨道类型是__________,SiF4微粒的空间构型是__________。又知若有d轨道参与杂化,能大大提高中心原子成键能力。试解释为什么BF3、SiF4水解的产物中,除了相应的酸外,前者生成BF4一后者却是生成SiF62—:______________________________________________。
(4)科学家发现硼化镁在39K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。下图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据图示确定硼化镁的化学式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ?ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ?ΔH=-192.9 kJ/mol
根据上述反应,下列说法正确的是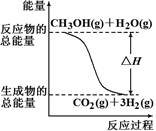
| A.反应①中的能量变化如上图所示 |
| B.可推知2H2(g)+O2(g)=2H2O(g)?ΔH=-483.8 kJ/mol |
| C.1 mol CH3OH充分燃烧放出的热量为192.9 kJ |
| D.CH3OH转变成H2的过程一定要吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应既是氧化还原反应,又是吸热反应的是( )
| A.铝片和稀硫酸反应 | B.Ba(OH)2?8H2O与NH4Cl反应 |
| C.灼热的炭与CO2反应 | D.甲烷在O2中燃烧 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com