
【题目】已知Ksp(CaCO3)=3.36×10—9,Ksp(CaF2)=3.45×10—11。下列关于CaCO3和CaF2两悬浊液说法错误的是
A. CaCO3悬浊液中c(Ca2+)较小
B. 分别滴加稀硫酸,溶度积常数均增大
C. 分别加入0.1mol/L的CaCl2溶液,c(CO32—)和 c(F—)均减小
D. CaF2更容易转化成CaCO3
【答案】B
【解析】
A. Ksp(CaCO3)=3.36×10—9,CaCO3悬浊液中c(Ca2+)=![]() mol/L,Ksp(CaF2)=3.45×10—11,CaF2悬浊液中c(Ca2+)=
mol/L,Ksp(CaF2)=3.45×10—11,CaF2悬浊液中c(Ca2+)=![]() mol/L,所以CaCO3悬浊液中c(Ca2+)较小,故正确;
mol/L,所以CaCO3悬浊液中c(Ca2+)较小,故正确;
B. 溶度积常数只受温度影响,故分别滴加稀硫酸,溶度积常数都不变,故错误;
C. 分别加入0.1mol/L的CaCl2溶液,钙离子浓度增大,所以溶解平衡逆向移动,则c(CO32—)和 c(F—)均减小,故正确;
D. 虽然Ksp(CaF2) <Ksp(CaCO3),但根据A项计算,碳酸钙的溶解度小于氟化钙,所以CaF2容易转化成更难溶的CaCO3,故正确。
故选B。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】将适量铁粉放入FeCl3溶液中,完全反应后,溶液中的Fe2+和Fe3+溶度相等,则未反应的Fe3+和已反应的Fe3+的物质的量之比是( )
A.2 :3B.3 :2C.1 :2D.1 :1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是( )
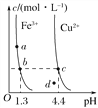
A. Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B. 加适量NH4Cl固体可使溶液由a点变到b点
C. c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
D. Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既不属于氧化还原反应,又是吸热反应的是( )
A. 铝片与稀盐酸的反应 B. Ba(OH)28H2O与NH4Cl的反应
C. 生石灰与水反应 D. 甲烷在氧气中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中符合图像的是 ( )

A. N2(g)+3H2(g)![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
B. 2SO3(g)![]() 2SO2(g)+O2(g)ΔH>0
2SO2(g)+O2(g)ΔH>0
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)ΔH<0
4NO(g)+6H2O(g)ΔH<0
D. H2(g)+CO(g)![]() C(s)+H2O(g) ΔH>0
C(s)+H2O(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能
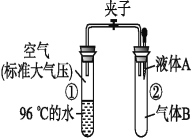
A. NaOH溶液、CO2
B. H2O、氨气
C. NaOH溶液、CO
D. H2O、NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质](15分)A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、 D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是 (填元素符号),其中C原子的核外电子排布式为__________。
(2)单质A有两种同素异形体,其中沸点高的是 (填分子式),原因是 ;A和B的氢化物所属的晶体类型分别为 和 。
(3)C和D反应可生成组成比为1:3的化合物E, E的立体构型为 ,中心原子的杂化轨道类型为 。
(4)化合物D2A的立体构型为 ,中心原子的价层电子对数为 ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为 。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm, F 的化学式为 :晶胞中A 原子的配位数为 ;列式计算晶体F的密度(g.cm-3) 。
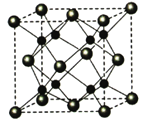
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com