
【题目】A、B、C、D四种短周期元素,0.5molA的元素的离子得到NA个电子后被还原为中性原子;0.4gA的氧化物恰好与100mL0.2mol/L的盐酸完全反应;A元素原子核内质子数与中子数相等.B元素原子核外电子数比A元素原子核外电子数多1;C﹣离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层电子数的2倍.(1)A元素的符号;(2)B的单质;C;D .
【答案】Mg;Al;Cl;C
【解析】解:短周期元素A、B、C、D中,0.5mol A元素的离子得到NA个电子被还原为中性原子,则A离子为带2个单位正电荷的阳离子,0.4g A的氧化物恰好与100ml 0.2mol/L的盐酸完全反应,由AO+2HCl═ACl2+H2O,可知M(AO)= ![]() =40g/mol,所以A的摩尔质量为40g/mol﹣16g/mol=24g/mol,又A原子核内质子数目与中子数目相等,则质子数为12,即A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al.Cˉ离子核外电子层数比A元素的离子核外电子层数多1,Cˉ离子核外电子数为18,故C为Cl元素;D元素原子最外层电子数是最内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,则D为C元素.(1)由上述分析可知,A、B、C、D四种元素符号分别为:Mg、Al、Cl、C,所以答案是:Mg;(2)B的单质是铝单质;C是氯气;D是碳单质,所以答案是:Al、Cl、C.
=40g/mol,所以A的摩尔质量为40g/mol﹣16g/mol=24g/mol,又A原子核内质子数目与中子数目相等,则质子数为12,即A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al.Cˉ离子核外电子层数比A元素的离子核外电子层数多1,Cˉ离子核外电子数为18,故C为Cl元素;D元素原子最外层电子数是最内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,则D为C元素.(1)由上述分析可知,A、B、C、D四种元素符号分别为:Mg、Al、Cl、C,所以答案是:Mg;(2)B的单质是铝单质;C是氯气;D是碳单质,所以答案是:Al、Cl、C.


科目:高中化学 来源: 题型:
【题目】甲、乙两化学兴趣小组安装两套如图1相同装置,用以探究影响H2O2分解速率的因素. 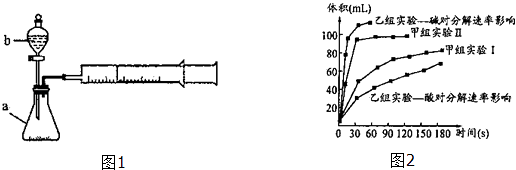
(1)仪器b的名称: .
(2)甲小组有如下实验设计方案,请帮助完成下列填空.
实验编号 | 实验目的 | t℃ | 催化剂 | 浓度 |
甲组实验Ⅰ | 做实验参照 | 25 | 10mL 2%H2O2 | |
甲组实验Ⅱ | 探究浓度对速率的影响 | 25 | 10mL 5%H2O2 |
(3)甲、乙两小组得出如图2数据. ①由甲组实验得出的数据可知:浓度越大,H2O2分解速率(填“越快”、“越慢”);
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析相同条件下,Na2O2和K2O2溶于水放出气体速率较快的是;
③乙组提出可以用BaO2固体与H2SO4溶液反应制H2O2 , 其化学反应方程式为;支持这一方案的理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚硫酸钠在空气中能被氧气氧化生成硫酸钠.某同学为探究Na2SO3溶液是否发生变质,设计如下实验测定1.0molL﹣1Na2SO3溶液的实际浓度. 
(1)分液漏斗中应加入足量的下列哪种试剂?(填选项)
A.浓硝酸
B.65%硫酸
C.浓盐酸
(2)实验前后C装置增重3.2g,则测得Na2SO3溶液的物质的量浓度为molL﹣1 .
(3)该实验装置还存在一个明显的缺陷是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关金属性质的叙述正确的是( )
A.都具有很高的熔点
B.最外层电子数少于 3 个的都是金属
C.都能导电、传热
D.都只能和酸不能和碱发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.苹果属于碱性食物
B.生铁和钢是含碳量不同的两种铁碳合金
C.亚硝酸钠是有毒物质,不能添加到食物中
D.处理含有重金属离子的废水常常综合应用氧化还原法和沉淀法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中加入铝片有氢气产生,则该溶液中一定能大量共存的离子组是( )
A.Cl﹣、Fe3+
B.HCO3﹣、Al3+
C.Ba2+、SO42﹣
D.Na+、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电﹣Fenton法是用于水体里有机污染物降解的高级氧化技术,其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2=Fe3++OH﹣+OH,生成的烃基自由基(OH)能氧化降解有机污染物.下列说法不正确的是( ) 
A.电源的A极是负极
B.电解池中只有O2、Fe3+发生还原反应
C.阳极上发生电极反应:H2O﹣e﹣=OH+H+ ,
D.消耗1molO2 , 可以产生4molOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com