
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,能生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为 ,B为 ,C为 ,D为 。(填元素符号)
(2)D的最高价氧化物的水化物的化学式是 ,E的电子式是 。
(3)写出由A、B组成的化合物与E反应的化学方程式: 。
(4)请用电子式表示出C和D形成的化合物F的形成过程: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
I.(10分)四种短周期元素X、Y、Z、W,原子序数依次增大,请结合表中
信息回答下列问题。
| X | Y | Z | W | |
| 结构 或 性质 | X的最高价氧化物对应的水化物与其气态氢化物反应可得到一种盐 | 焰色反应呈黄色 | 在同周期主族元素形成的简单离子中,Z的离子半径最小 | 原子核外最外层电子数是次外层电子数的一半 |
(1)用电子式表示X的氢化物的形成过程_____________________________。
(2)W元素在周期表中的位置为____________________。
(3)上述元素的最高价氧化物对应的水化物中,有一种物质甲与其它三种物质在一定条件下均能发生化学反应,则甲中所含的化学键有________(填序号)。
a.离子键 b.极性共价键 c.非极性共价键 d.氢键
(4)向含有Z元素的简单阳离子的溶液中加入过量的NaOH溶液,发生反应的离子方程式为_____________________________________。
(5)下列可作为比较Z和Mg金属性强弱的方法是_______(填代号)。
a.比较两种元素在化合物中化合价的高低
b.测等浓度相应氯化物水溶液的pH
c.在常温条件下比较单质与浓硝酸反应的剧烈程度
d.在两种金属氯化物的水溶液中分别滴加过量的NaOH溶液
II.(8分)多种物质的转化关系如下图所示(部分反应物或产物已略去,反应条件未列出):

已知:①A、B、C、D、G含有同种元素,且它们的状态与颜色如下表
所示:

②E是通常情况下密度最小的气体;B与AgNO3生成不溶于稀硝酸的白色沉淀;一种气体氧化物M通入B溶液中可被氧化为F,F是含有三种元素的共价化合物,F与A反应生成E和G。
请回答下列问题:
(1)写出下列物质的化学式:D___________;E__________。
(2)写出下列反应的离子方程式:
①B+M→F:________________________________________;
②A+F→E+G:______________________________________。
(3)下列氧化物中能与G溶液反应直接生成C固体的是_______(填字母)。
a.Na2O2 b.SO2 c.CO2 d.BaO2
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应过程中体系的能量变化如图所示,下列说法错误的是
A.反应过程可表示为A+BC—→[A…B…C] —→AB+C
(反应物) (过渡态) (产物)
B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
C.正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应
D.此图中逆反应的热效应△H=E1—E2,为吸热反应

查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下:
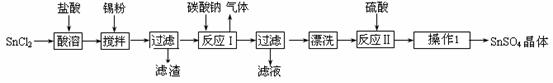
查阅资料:Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡。请回答下列问题:
(1)操作Ⅰ步骤是 ▲ 。
(2)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因 ▲ 。
(3)加入Sn粉的作用有两个:①调节溶液pH ② ▲ 。
(4)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是 ▲ 。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 ▲ 。
(6)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl===SnCl2 + H2↑;
②加入过量的FeCl3溶液;
③用已知浓度的K2Cr2O7滴定②中生成的Fe2+,发生的反应为:
6FeCl2 + K2Cr2O7 + 14HCl ===6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1.190 g 锡粉,经上述各步反应后,共用去0.100 mol/L K2Cr2O7溶液25.00 mL。锡粉中锡的质量分数是 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
A.M与X形成的化合物对应的水化物一定是强酸
B.Y2X和Y2X2中化学键类型完全相同
C.X、Y的简单离子半径:r(X2-)>r(Y+)
D.M的气态氢化物比N的气态氢化物稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表是学习物质结构与性质的重要工具。下表是元素周期表的一部分,表中所列字母A、B、D、E、G、H、Q、M、R分别代表某一化学元素。请用所给元素回答下列问题。
| A | |||||||||||||||||
| M | B | D |
| ||||||||||||||
| G | H |
|
| Q | R | ||||||||||||
| E |
| ||||||||||||||||
(1)Q元素在元素周期表中的位置 ,E元素原子结构示意图为
(2)E、Q、R三种元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是(填离子符号)_________________________________。
(3)M、D两元素形成的化合物中含有的化学键类型是 ,其MD2分子的结构式:
(4)用电子式表示物质GDA_________________; 用电子式表示G与Q形成化合物的过程 ;
(5)用表中所给元素组成反应物,请各用一个化学方程式说明元素Q和R非金属性的强弱: ;元素G、H的金属性强弱:
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值,下列说法正确的是
( )。
A.25 ℃时,pH=2的1.0 L H2SO4溶液中含有H+的数目为0.02 NA
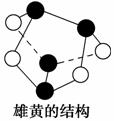
B.0.5 mol雄黄(As4S4,所有原子都满足8电子结构, 结构如图)含有NA个S—S键
结构如图)含有NA个S—S键
C.39 g苯分子中共含6 NA个共价单键
D.向FeI2、NaBr的混合溶液中通入适量氯气,当有1 mol Fe2+被氧化时,该反应转移电子的数目至少为3 NA
mol Fe2+被氧化时,该反应转移电子的数目至少为3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程的离子方程式正确的是
A.用烧碱溶液吸收Cl2:Cl2+2OH- =Cl-+ClO-+H2O
B.用饱和Na2CO3溶液转化锅垢中的CaSO4:CaSO4(s)+CO32- (aq)=CaCO3(s)+SO42-(aq)
C.实验室制备Fe(OH)3胶体:Fe3+ +3OH- =Fe(OH)3↓
D.金属Na与水反应:Na +2H+ = H2↑+Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com