
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.C2H4和HCN分子中,都含σ键和π键,但C原子的杂化方式并不相同
B.在元素周期表中,p区元素的最外层电子排布均可表示为ns2np1~6
C.某基态原子的核外电子排布图为 ,它违背了泡利不相容原理
,它违背了泡利不相容原理
D.用红外光谱可鉴别乙醇和二甲醚,用X-射线衍射实验可鉴别玻璃与水晶
查看答案和解析>>
科目:高中化学 来源: 题型:
已知室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3。向浓度均为0.1 mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是 ( )


查看答案和解析>>
科目:高中化学 来源: 题型:
元素的性质呈现周期性变化的根本原因是 ( )
A.原子半径呈周期性变化 B.元素的化合价呈周期性变化
C.第一电离能呈周期性变化 D.元素原子的核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列晶体分类中正确的一组是( )
| 选项 | 离子晶体 | 原子晶体 | 分子晶体 | 金属晶体 |
| A. | NH4Cl | Ar | C6H12O6 | 生铁 |
| B. | H2SO4 | Si | S | Hg |
| C. | CH3COONa | SiO2 | I2 | Fe |
| D. | Ba(OH)2 | 石墨 | 普通玻璃 | Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2H2(g)+O2(g)===2H2O(l);ΔH=-569.6 kJ·mol-1,
2H2O(g)===2H2(g)+O2(g);ΔH=+482.1 kJ·mol-1。
则1 g液态H2O蒸发时吸收的热量是( )
A.2.43 kJ B.4.86 kJ C.43.8 kJ D.87.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
“人文奥运、科技奥运、绿色奥运”是2008年北京奥运会的重要特征。其中禁止运动员使用兴奋剂是重要举措之一。以下两种兴奋剂的结构分别为:


①利尿酸 ②兴奋剂X
则关于它们的说法中正确的是( )
A.利尿酸乙酯分子中有三种含氧官能团,在核磁共振氢谱上共有七个峰
B.1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2
C.两种兴奋剂最多都能和含3molNaOH的溶液反应
D.两种分子中的所有碳原子均不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)碳、氮广泛的分布在自然界中,碳、氮的化合物性能优良,在工业生产和科技领域有重要用途。
(1)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300~1700oC的氮气流中反应制得:3SiO2(s)+6C(s)+2N2(g)  Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
Si3N4(s)+6CO(g)。⊿H =-1591.2 kJ/mol,则该反应每转移1mole—,可放出的热量为 。
(2)某研究小组现将三组CO(g)与H2O(g)的混合气体分别通入体积为2L的恒容密闭容器中,一定条件下发生反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:

① 实验Ⅰ中,前5min的反应速率v(CO2)= 。
②下列能判断实验Ⅱ已经达到平衡状态的是 。
a.容器内CO、H2O、CO2、H2的浓度不再变化 b.容器内压强不再变化
c.混合气体的密度保持不变 d.v正(CO) =v逆(CO2)
e.容器中气体的平均相对分子质量不随时间而变化
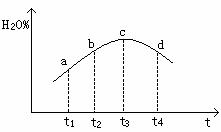
③若实验Ⅲ的容器是绝热的密闭容器,实验测得H2O(g)的转化率H2O%随时间变化的示意图如下图所示, b点v正 v逆(填“<”、“=”或“>”),t3~t4时刻,H2O(g)的转化率H2O%降低的原因是 。
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式 ,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH= (溶液电解前后体积的变化忽略不计)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com