
【题目】“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( ) 
A.加热时,①上部汇聚了固体碘,说明碘的热稳定性较差
B.加热时,②、③中的溶液均变红,冷却后又都变为无色
C.④中,浸泡在热水中的容器内气体颜色变深,浸泡在冰水中的容器内气体颜色变浅
D.四个“封管实验”中都有可逆反应发生
【答案】C
【解析】解:A.加热时,①上部汇集了固体碘单质,说明碘发生了升华现象,为其物理性质,不能说明碘单质的热稳定性较差,故A错误; B.②中氨水显碱性,使酚酞变红,加热时,氨气逸出,冷却后,氨气又和水反应,变成红色,二氧化硫与品红显无色,加热后二氧化硫逸出,显红色,二者现象不同,故B错误;
C.2NO2(g)N2O4(g)△H=﹣92.4kJ/mol,正反应为放热反应,升高温度平衡向逆反应方向移动,则颜色变深,④中浸泡在热水中的容器内气体颜色变深,反之变浅,所以浸泡在冰水中的容器内气体颜色变浅,故C正确;
D.氯化铵受热分解与氨气和氯化氢反应生成氯化铵不是可逆反应,因前者须加热,后者只要在常温下,故D错误;
故选C.


科目:高中化学 来源: 题型:
【题目】在塑料袋中放一个成熟的苹果和一些青香蕉,将袋口密封,两天后青香蕉成熟了。导致青香蕉成熟的物质是成熟苹果释放出的
A. C2H4 B. CH3COOH C. C6H6 D. CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.10gT2O含有的电子数为5NA
B.常温下,0.2L 0.5molL﹣1NH4NO3溶液的氮原子数小于0.2NA
C.用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.4NA
D.常温常压下,5.6gC2H4和C3H6的混合气体中含氢原子数为0.9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液.由该废液回收铜并得到净水剂(FeCl36H2O)的步骤如下:Ⅰ.在废液中加入过量铁粉,过滤;
Ⅱ.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
Ⅲ.合并Ⅰ和Ⅱ中的滤液,通入足量氯气;
Ⅳ.…,得到FeCl36H2O晶体.
(1)用FeCl3溶液腐蚀铜箔的离子方程式是 .
(2)试剂A是 .
(3)步骤Ⅲ中发生的离子方程式为 .
(4)完成步骤Ⅳ需要用到的实验装置是(填字母).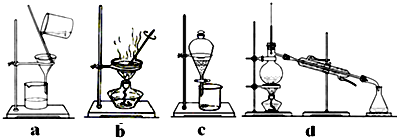
(5)若用FeCl36H2O晶体配制100ml 0.5mol/L的FeCl3溶液①用托盘天平称FeCl36H2O晶体,其质量是g.
②实验时下图所示操作的先后顺序为(填编号).
蒸馏水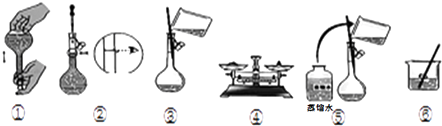
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中因有配离子生成而不能大量共存的是( )
A. K+、Na+、Cl-、NO3-B. Mg2+、Ca2+、SO42-、OH-
C. Fe2+、Fe3+、H+、NO3-D. Ba2+、Fe3+、Cl-、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚甲基丙烯酸羟乙酯的结构简式为  ,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式:
,它是制作软质隐形眼镜的材料.请写出下列有关反应的化学方程式:
(1)由甲基丙烯酸羟乙酯制备聚甲基丙烯酸羟乙酯
(2)由甲基丙烯酸制备甲基丙烯酸羟乙酯
(3)由乙烯制备乙二醇 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】XeO3是一种不稳定的物质,具有强氧化性.
(1)配平反应的离子方程式:
XeO3+Mn2++H2O→MnO4﹣+Xe↑+H+
(2)反应现象为:①有气泡产生;② .
(3)被氧化的元素是 .
(4)将适量的XeO3投入30mL 0.1molL﹣1 Mn2+的水溶液中,刚好完全反应.
①此时转移电子总数为 .
②将反应后的溶液稀释至90mL,所得溶液的pH= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为铜丝与浓硫酸反应并验证其产物性质的实验装置.
(1)①中反应的化学方程式是 , 其中铜发生了(填“氧化”或“还原”)反应,判断依据为 .
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸.加热一段时间后,③中溶液依然澄清,④中溶液褪色.想要立即终止铜与硫酸的反应,最恰当的方法是 . a.上移铜丝,使其脱离硫酸
b.撤去酒精灯
c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
加入试剂 | 现象 | 反应的离子方程式 | |
第一份 | 加入NaOH溶液 | 有白色沉淀生成 | |
第二份 | 加入氯水 | 有白色沉淀生成 |
完成上述反应的离子方程式.
(4)④中棉花团的作用是 .
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色.取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭可以转化为清洁能源和化工原料.
(1)用煤可以制得水煤气.工业上可用煤和水通过水煤气法制氢气,已知下列热化学方程式:
C(s)+ ![]() O2(g)═CO(g)△H1=﹣110.5kJmol﹣1
O2(g)═CO(g)△H1=﹣110.5kJmol﹣1
2H2(g)+O2(g)═2H2O(g)△H2=﹣483.6kJmol﹣1
试求水煤气法制氢气的反应的反应热△H3 .
C(s)+H2O(g)═CO(g)+H2(g)△H3=kJmol﹣1
(2)若H﹣H、O=O和O﹣H键的键能分别是436kJmol﹣1、496kJmol﹣1和m kJmol﹣1 , 结合上述热化学方程式的相关数据计算,m= .
(3)已知一氧化碳与水蒸气反应过程的能量变化如图所示:则此反应为(填“吸热”或“放热”)反应,反应的热化学方程式为 . 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com