
【题目】某校同学在实验室中对一氧化碳与硫酸钙反应进行了探究。回答下列问题:
(1)甲组同学利用CaSO4·2H2O在400--500℃脱水制取无水CaSO4。实验中需用到的加热装置中的硅酸盐质的仪器除玻璃棒外,还用到______________。
(2)乙组同学利用H2C2O4·2H2O在浓硫酸作用下脱水生成CO、CO2并制备纯净的CO气体,实验装置如下:
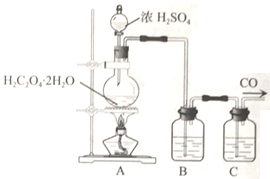
B、C中盛放的试剂依次为______、____________。
(3)丙组同学利用甲组制得的无水CaSO4和乙组制得的CO并利用下列装置验证反应并检验气态产物中有SO2和CO2产生。
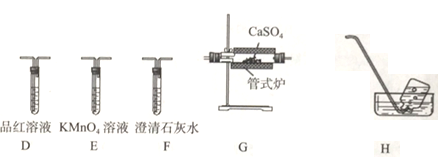
①上述装置(部分装置可重复使用)的连接顺序为C→___________。
②若E溶液褪色,则发生反应的离子方程式为_____________。
③能证明有CO2的生成的实验依据是____________。
④若G中产物为CaO,则G中发生反应的化学方程式为_________________。
(4)丁组的同学取丙组实验后G装置中的固体产物加入试管中,然后加人足量稀盐酸,固体完全溶液且产生少量气体,通入CuSO4溶液有黑色沉淀。可验证CO与CaSO4在高温下还发生了一个副反应,该反应为______________(用方程式表示)。
【答案】 坩埚和泥三角 浓NaOH溶液 浓硫酸 G →D→E→D→F→H 5SO2 +2MnO4-+2H2O = 2Mn2++5SO42-+ 4H+ D中品红溶液不褪色,其后的澄清石灰水变浑浊 CaSO4 + CO![]() CaO + SO2+CO2 CaSO4 + 4CO
CaO + SO2+CO2 CaSO4 + 4CO![]() CaS +4CO2
CaS +4CO2
【解析】(1)甲组同学利用CaSO4·2H2O在400--500℃脱水制取无水CaSO4,因为温度较高,所以要用到坩埚,附加仪器泥三角都属于硅酸盐质的仪器。故答案:坩埚和泥三角。
(2)因为H2C2O4·2H2O在浓硫酸作用下脱水生成CO、CO2,要制得纯净的CO气体,就必须除去CO2 H2O,由实验装置知B为除去CO2,C除去水,所以B中加浓NaOH溶液 C中加.浓硫酸。答案:浓NaOH溶液 浓硫酸。
(3)因无水CaSO4要和CO反应会产生SO2和CO2,检验SO2和CO2的顺序为检验SO2![]() 除去SO2
除去SO2![]() 验证是否除净
验证是否除净![]() 检验CO2。
检验CO2。
①根据所给装置(部分装置可重复使用)的连接顺序为G→D→E→D→F→H。
②若E溶液褪色,是SO2和高锰酸钾溶液反应,则发生反应的离子方程式为5SO2 +2MnO4-+2H2O = 2Mn2++5SO42-+ 4H+
③能证明有CO2的存在是使澄清的,因为SO2也能使石灰水变浑浊,所以要先除去SO2,故能证明有CO2的生成的实验依据是D中品红溶液不褪色,其后的澄清石灰水变浑浊。
④若G中产物为CaO,根据③知产物为CO2和 SO2,,则G中发生反应的化学方程式为CaSO4 + CO![]() CaO + SO2+CO2 。
CaO + SO2+CO2 。
(4)丁组的同学取丙组实验后G装置中的固体产物加入试管中,然后加人足量稀盐酸,固体完全溶液且产生少量气体,通入CuSO4溶液有黑色沉淀的气体为H2S。是G装置中的固体产物加入稀盐酸产生的H2S,所以固体物质中含有硫化物,故CO与CaSO4在高温下发生的副反应为CaSO4 + 4CO![]() CaS +4CO2。
CaS +4CO2。


科目:高中化学 来源: 题型:
【题目】如图示是由3个圆所构成的类别关系图,其中I为大圆,II和III分别为大圆之内的小圆。下列选项中符合这种类别关系的是( )

A. I: DNA II: RNA III:核酸
B. I:还原性糖 II:果糖 III:蔗糖
C. I:固醇 II:胆固醇 III:维生素D
D. I:蛋白质 II:酶 III:激素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰及其化合物在生产、生活中有许多用途。在实验室中模拟工业利用软锰矿(主要成分为MnO2,含少量SiO2、Fe2O3和Al2O3等)制备金属锰等物质,设计流程如下:

己知:Mn2+有较强的还原性,在空气中能被氧气氧化,碳酸锰在空气中高温加热固体产物为Mn2O3;部分氢氧化物的Ksp(近似值)如下表。
物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
Ksp | 10-13 | 10-17 | 10-39 | 10-33 |
(1)“酸浸”前需将软锰矿粉碎的目的是_____________;酸浸过程MnO2发生反应的离子方程式为_________________。
(2)向滤液I中需先加A物质,再加B物质,若加入的物质均为非金属化合物的溶液,则A为(填物质的名称)_________,B为(填物质的名称)________。滤渣II的成分是_______(填物质的化学式)。
(3)“酸浸”需适宜的酸浓度、液固比、酸浸温度等,其中浸取率随酸浸时间的变化如图所示:

当浸取时间超过4h时,锰浸取率反而减小,其原因是______________。
(4)测得滤液I中c(Mn2+)=0.1mo/L,则加入B调节溶液pH范围为______。(已知:当某种离子浓度小于1×10-5mo/L时,可认为其沉淀完全。结果保留两位小数)
(5)“沉锰”过程中加入氨水的目的是(从化学平衡移动的角度解释)______________。
(6)写出由MnCO3为原料制备金属锰的过程中所涉及的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《天工开物》中记载了古人冶金、制陶瓷、硫磺、火药等的过程,是我国古代闪耀的“科技之光”,下列冶炼铁的过程中发生化学变化的是
A.凡铁场所在有之,其铁浅浮土面,浮者拾之 | B.取来淘洗 | C.入炉熔化 | D.凡铁一炉载土二千余斤,或用硬木柴,或用煤炭,或用木炭,土化成铁 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)

(1)第①步中,操作A是________,第⑤步中,操作B是________。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)______________。
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是__________。
(4)判断BaCl2已过量的方法是____________________________________。
(5)下列是某学生设计操作A后混合液中Cl-、SO42-的检验步骤请根据内容填空:
①首先检验_____离子,应先加入过量的_____________________。
②将所得混合物______(填操作名称),然后在溶液中加入试剂________检验另一离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作(注意事项)中,是基于实验安全考虑的是( )
①加热盛有液体的烧瓶时,需加碎瓷片或沸石
②酒精灯内的酒精不能小于酒精灯容积的三分之一
③实验前,要对气体实验装置进行气密性检査
④稀释浓硫酸时,将浓硫酸沿烧杯内壁慢慢注入水中
⑤实验结束后,清洗后的洁净试管,要倒放在试管架上
A. ①②③④⑤ B. ①②④ C. ②③④ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验基本操作(注意事项)中,是基于实验安全考虑的是( )
①加热盛有液体的烧瓶时,需加碎瓷片或沸石
②酒精灯内的酒精不能小于酒精灯容积的三分之一
③实验前,要对气体实验装置进行气密性检査
④稀释浓硫酸时,将浓硫酸沿烧杯内壁慢慢注入水中
⑤实验结束后,清洗后的洁净试管,要倒放在试管架上
A. ①②③④⑤ B. ①②④ C. ②③④ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂醛F(![]() )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
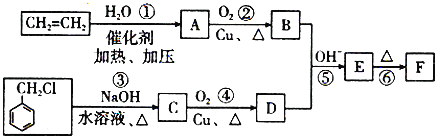
已知两个醛分子在NaOH溶液作用下可以发生反应,生成一种羟基醛:
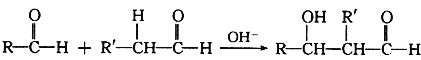
请回答:
(1)D的结构简式为______.
(2)反应①~⑥中属于加成反应的是______(填序号).
(3)写出有关反应③的化学方程式:___________.
(4)在实验室里鉴定![]() 分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是______(请按实验步骤操作的先后次序填写序号).
分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是______(请按实验步骤操作的先后次序填写序号).
A.滴加AgNO3溶液B.加NaOH溶液C.加热D.用稀硝酸酸化
(5)E物质的同分异构体有多种,其中符合条件:苯环上有两个取代基,其中一个是羧基的为:______(写出其中一种同分异构体的结构简式即可).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com