
【题目】下列反应中,属于氧化还原反应同时又是吸热反应的是
A.Ba(OH)2·8H2O与NH4Cl反应
B.铝与稀盐酸
C.灼热的炭与水蒸气生成一氧化碳和氢气的反应
D.煤与O2的燃烧反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷,它受热易分解,为了验证其气态产物,某同学设计了如下实验装置:
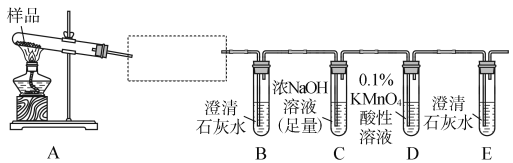
(1)若实验中,观察到B、E中的溶液均变浑浊,则D中的现象是_______________________;
说明其气态产物是________、________;为验证另一种气态产物,应在A、B之间增加的装置为________。
(2)为了使实验更安全、更严密,你认为该实验设计需要如何改进?
①______________________________;
②__________________________________。
(3)固体产物中铁元素不可能以+3价形式存在,理由是___________________________。
现设计实验,探究固体产物中铁元素的存在形式。
①提出合理假设。
假设1:_________________________________;
假设2:_________________________________;
假设3:_________________________________。
②某学生设计实验探究上述假设,除3%H2O2、蒸馏水外,还需要下列试剂中的____________________________。
限选试剂:浓硫酸、1.0 mol·L-1HNO3、1.0 mol·L-1盐酸、1.0 mol·L-1NaOH溶液、0.1 mol·L-1KI溶液、0.1 mol·L-1CuSO4溶液、20%KSCN溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Na2CO3和NaHCO3混合物灼烧至恒重,将放出的气体通入足量的澄清石灰水中,充分反应后得到的沉淀的质量是l.0g,加热后剩余的固体物质与足量的稀盐酸反应,收集到1.12L气体(标准状况).则原固体混合物中NaHCO3的物质的量为_______,Na2CO3的质量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH![]() 、Fe3+、AsO
、Fe3+、AsO![]() 、Cl-。为除去杂质离子,部分操作流程如下:
、Cl-。为除去杂质离子,部分操作流程如下:
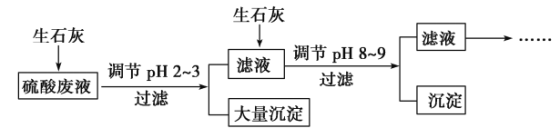
请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9 g·L-1,则该溶液中的pH约为_____________________________。
(2)NH![]() 在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在。现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH
在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在。现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH![]() )恰好是NH4Cl溶液中c(NH
)恰好是NH4Cl溶液中c(NH![]() )的2倍,则c[(NH4)2SO4]__________c(NH4Cl)(填“<”“=”或“>”)。
)的2倍,则c[(NH4)2SO4]__________c(NH4Cl)(填“<”“=”或“>”)。
(3)随着向废液中投入生石灰(忽略溶液温度的变化),溶液中![]() __________(填“增大”“减小”或“不变”)。
__________(填“增大”“减小”或“不变”)。
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4·2H2O[含有少量Fe(OH)3],提纯CaSO4·2H2O的主要操作步骤:向沉淀中加入过量________,充分反应后,过滤、洗涤、__________________________。
(5)25 ℃,H3AsO4电离常数为K1=5.6×10-3,K2=1.7×10-7,K3=4.0×10-12。当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2。
①pH调节到8左右Ca3(AsO4)2才开始沉淀的原因是_____________________。
②Na3AsO4第一步水解的平衡常数数值为___________________。
③已知:AsO![]() +2I-+2H+===AsO
+2I-+2H+===AsO![]() +I2+H2O,SO2+I2+2H2O===SO
+I2+H2O,SO2+I2+2H2O===SO![]() +2I-+4H+。上述两个反应中还原性最强的微粒是__________。
+2I-+4H+。上述两个反应中还原性最强的微粒是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com