
【题目】一定温度下,10 mL 0.4 mol/LH2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表:
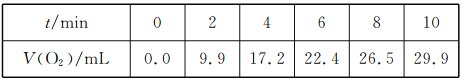
下列叙述错误的是(溶液体积变化忽略不计)( )
A.反应至6 min时,c(H2O2)=0.20mol/L
B.反应至6 min时,H2O2分解了40%
C.0~6 min的平均反应速率:v(H2O2)≈3.3×10-2 mol.L-1.min-l
D.6~10 min的平均反应速率:可(H2O2) <3.3×10-2 mol.L-1.min-l
【答案】B
【解析】
试题分析:2H2O2=2H2O+O2↑,A、6min产生氧气的体积为22.4×10-3L,消耗的H2O2的物质的量为22.4×10-3×2/22.4mol=2×10-3mol,因此剩余H2O2的浓度为(10×10-3×0.4-2×10-3)/10×10-3mol·L-1=0.2mol·L-1,故说法正确;B、根据选项A的分析,过氧化氢的分解率为2×10-3/10×10-3×0.4×100%=50%,故说法错误;C、根据反应速率定义,v(H2O2)=2×10-3/(10×10-3×6)mol/(L·min)=3.3×10-2 mol/(L·min),故说法正确;D、随着反应进行,浓度减少,反应速率降低,故说法正确。


科目:高中化学 来源: 题型:
【题目】下表是常温下某些一元弱酸的电离常数,则0.1 mol·L-1的下列溶液中,pH最小的是( )
弱酸 | HCN | HF | CH3COOH | HNO2 |
电离常数 | 4.9×10-10 | 7.2×10-4 | 1.8×10-5 | 6.4×10-6 |
A.HCN B.HF C.CH3COOH D.HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F均为短周期元素,且原子序数依次增大,A是原子半径最小的元素,B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4∶1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成离子个数比为2∶1的离子化合物丙。
(1)E在周期表中的位置为 。
(2)下列说法正确的有 。
①化合物乙分子中只含有极性共价键
②C、D、E、F原子半径由大到小的顺序为C>D>E>F
③B、E形成的氢化物中,B的氢化物更稳定
④化合物甲和化合物丙都含有离子键和共价键
(3)将F燃烧的产物通入BaCl2和HNO3的混合溶液中,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应 。
(4)写出一个由以上元素构成的10电子微粒与18电子微粒反应的离子方程式 。
(5)A与B可形成一种二元化合物X,其中A元素质量分数为2.33%.据研究X显弱酸性。回答:
①X的电离方程式为 __。
②X电离的阴离子结构与二氧化碳相似,则其电子式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分散系最不稳定的是( )
A. 向CuSO4溶液中加入NaOH溶液得到的分散系
B. 向水中加入食盐得到的分散系
C. 向沸水中滴入饱和FeCl3溶液得到的红褐色液体
D. 向NaOH溶液中通入CO2得到的无色溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2Zn(OH)2ZnCO3是制备活性ZnO的中间体,以锌焙砂(主要成分为ZnO,含少量Cu2+、Mn2+等离子)为原料制备2Zn(OH)2ZnCO3的工艺流程如下:
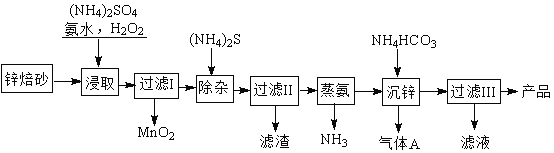
请回答下列问题:
(1)当(NH4)2SO4,NH3·H2O的混合溶液中存在c(NH4+)=2c(SO42 - )时,溶液呈 (填“酸”、“碱”或“中”)性。
(2)“浸取”时为了提高锌的浸出率,可采取的措施是 (任写一种)。
(3)“浸取”时加入的NH3·H2O过量,生成MnO2的离子方程式为 。
(4)适量S2-能将Cu2+等离子转化为硫化物沉淀而除去,若选择ZnS进行除杂,是否可行?用计算说明原因: 。
[已知:Ksp(ZnS)=1.6×10-24,Ksp(CuS)=1.3×10-36]
(5)“沉锌”的离子方程式为 。
(6)“过滤3”所得滤液可循环使用,其主要成分的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池是化学电源,其电极材料分别是Pb和PbO2,电解质溶液为稀硫酸,工作时该电池的总反应式为Pb+PbO2+2H2SO4===2PbSO4+2H2O。试根据上述情况判断:
(1)蓄电池的负极材料是______________。
(2)工作时,正极反应为______________________________。
(3)工作时,电解质溶液的酸性__________(填“增大”“减小”或“不变”)。
(4)工作时,电解质溶液中阴离子移向____________极。
(5)电流方向从____________极流向____________极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活处处有化学。下列说法正确的是
A. 制饭勺、饭盒、高压锅等的不锈钢是合金
B. 做衣服的棉和麻均与淀粉互为同分异构体
C. 煎炸食物的花生油和牛油都是可皂化的饱和酯类
D. 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com