
X元素原子的核电荷数为n,X2-离子和Y3+离子的电子层结构相同,则Y原子的质子数为
A.n+1 B.n+2 C.n+3 D.n+5
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:实验题
(12分)现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL 0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④药匙 ⑤量筒 ⑥容量瓶 ⑦托盘天平。
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。配制时还欠缺的仪器是 。
(2)经计算,需浓H2SO4的体积为 mL(精确到0.1)。
(3)配制过程有以下操作:
A.移液
B.量取
C.洗涤
D.定容
E.溶解
F.摇匀
其正确的操作顺序应是 (填序号)。
(4)在配制过程中,其他操作都准确,下列操作中,能引起误差偏高的有 (填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②稀释后的H2SO4溶液未等冷却至室温就转移到容量瓶中
③定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
④转移前,容量瓶中含有少量蒸馏水
⑤定容时,俯视标线
(5)从上述容量瓶中移取25.00mL的稀硫酸溶液于100mL的容量瓶,加水稀释至刻度线。请问所得溶液中c(H+)= 。
(6)某研究小组欲利用氯气和二氧化硫通入水溶液中来制备100mL含0.4molH+的溶液,反应原理:Cl2+SO2+2H2O= H2SO4+2HCl,若忽略制备过程中气体的损耗,请问需标准状况下的氯气 L。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区八校高二上学期期中联考化学试卷(解析版) 题型:选择题
要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液
A.③① B.③② C.①③ D.①②③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区八校高二上学期期中联考化学试卷(解析版) 题型:选择题
在铝中加入某种金属可得到低密度,高强度的新型铝合金,可代替常规的铝合金用于制造航天飞机这种金属是
A.锂 B.镁 C.铜 D.锰
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区八校高一上学期期中联考化学试卷(解析版) 题型:选择题
铜有两种天然同位素63Cu和65Cu,已知铜元素的近似相对原子质量为63.5,则63Cu的原子个数百分数是
A.75% B.25% C.50% D.45%
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区八校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列关于摩尔的说法中,正确的是
A.是物质的量 B.是一个物理量
C.是一种物理量的单位 D.是摩尔质量
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高二上学期期中化学试卷(解析版) 题型:填空题
(14分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度 (mol·L-1) | 混合溶液的pH |
甲 | 0.2 | 0.2 | pH=a |
乙 | c1 | 0.2 | pH=7 |
丙 | 0.2 | 0.1 | pH>7 |
丁 | 0.1 | 0.1 | pH=9 |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸:_________________________________________________________。
(2)不考虑其他组的实验结果,单从乙组情况分析,c1是否一定等于0.2 mol·L-1?______(选填“是”或“否”)。混合溶液中离子浓度c(A-)与c(Na+)的大小关系是________。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是______酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是 ____________ 。
(4)写出丁组实验所得混合溶液中下列算式的精确结果(不能做近似计算)。
c(Na+) - c(A-)= ____________mol·L-1;
c(OH-) -c(HA)= ____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高二上学期期中化学试卷(解析版) 题型:选择题
已知C(金刚石) C(石墨)ΔH = - Q(Q>0),下列热化学方程式放出热量最多的是
C(石墨)ΔH = - Q(Q>0),下列热化学方程式放出热量最多的是
A.C(金刚石)+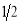 O2(g) =CO(g) ΔH = - Q1
O2(g) =CO(g) ΔH = - Q1
B.C(石墨)+ 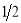 O2(g) =CO(g) ΔH = - Q2
O2(g) =CO(g) ΔH = - Q2
C.C(金刚石) + O2(g) =CO2(g) ΔH = - Q3
D.C(石墨)+ O2(g) =CO2(g) ΔH = - Q4
查看答案和解析>>
科目:高中化学 来源:2013~2014学年福建省第一学期高三第二次月考化学试卷(解析版) 题型:填空题
(15分)五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
(1)A原子核外电子总数是内层电子数的三倍,A、E同主族
(2)B的最高价氧化物对应的水化物F与其气态氢化物G反应,得到离子化合物H。
(3)C的焰色应呈黄色。
(4)D在同周期主族元素形成的简单离子中,离子半径最小.
回答下列问题:
(1)写出D在元素周期表中的位置:
(2)化合物H的水溶液pH 7 其原因是 (用离子方程式表示)
(3)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他四种物质发生化学反应,写出该物质的电子式
(4)某同学设计实验证明A、B、E的非金属性强弱关系。
①溶液a和b分别为 , 。
②溶液c中的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com