
【题目】下列关系的表述中,正确的是( )
A.0.1mol?L﹣1NaHSO4溶液中:c(Na+)+c(H+)=c(SO ![]() )+c(OH﹣)
)+c(OH﹣)
B.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1:1
C.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)不相等
D.0.1mol?L﹣1NaHCO3溶液中:c(Na+)>c(HCO ![]() )>c(CO
)>c(CO ![]() )>c(H2CO3)
)>c(H2CO3)
【答案】C
【解析】解:A、根据溶液中的电荷守恒:c(Na+)+c(H+)=2c(SO ![]() )+c(OH﹣),故A错误; B、盐酸和醋酸分别是强酸和弱酸,当PH相等时,醋酸的浓度大于盐酸,所以醋酸消耗的氢氧化钠要比盐酸多,故B错误;
)+c(OH﹣),故A错误; B、盐酸和醋酸分别是强酸和弱酸,当PH相等时,醋酸的浓度大于盐酸,所以醋酸消耗的氢氧化钠要比盐酸多,故B错误;
C、pH=3的盐酸中,水电离出的c(H+)=c(OH﹣)= ![]() =10﹣11 , pH=3的FeCl3溶液中,水电离的c(H+)=10﹣3 , 水电离的c(H+)不相等,故C正确;
=10﹣11 , pH=3的FeCl3溶液中,水电离的c(H+)=10﹣3 , 水电离的c(H+)不相等,故C正确;
D、在碳酸钠溶液中,钠离子和碳酸氢根是直接电离出的离子,但是碳酸氢根会水解和电离,所以c(Na+)>c(HCO ![]() ),碳酸氢钠中,碳酸氢根的水解程度大于电离程度,所以c(CO
),碳酸氢钠中,碳酸氢根的水解程度大于电离程度,所以c(CO ![]() )<c(H2CO3),
)<c(H2CO3),
离子浓度大小关系为:c(Na+)>c(HCO ![]() )>c(H2CO3)>c(CO
)>c(H2CO3)>c(CO ![]() ),故D错误.
),故D错误.
故选C.


科目:高中化学 来源: 题型:
【题目】某中学化学兴趣小组学生在学习“含硫化合物的性质和应用”时,进行了如下实验探究:为了验证浓硫酸和碳在加热的情况下反应的生成物,用图Ⅰ装置进行实验。

(1)请写出碳与浓硫酸反应的化学反应方程式_________________________________;该反应中氧化剂与还原剂的物质的量之比为_____________;
(2)图Ⅰ中A处是完成实验中的必要装置,它是下图所示中的_________;(填编号)
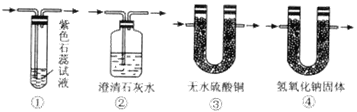
(3)图Ⅰ中C装置中应盛的试剂最好为:足够的_______________,其作用是__________________;
(4)若出现_______________________ 的实验现象,则可以确定存在二氧化碳气体。
(5)现实验小组的同学继续进行实验,他们将二氧化硫和氯气按一定的比例同时通入品红溶液中,一段时间后,发现品红溶液没有褪色。试分析实验过程中,品红不褪色的原因___________________(用离子反应方程式表示);你认为怎么样做可以让品红的颜色越来越浅?_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. 铝粉与NaOH溶液反应:Al + 2OH-===AlO![]() + H2↑
+ H2↑
B. SiO2和NaOH溶液反应:SiO2+ 2OH-===SiO![]() + H2O
+ H2O
C. 氯化铵浓溶液跟浓NaOH溶液混合后加热:NH![]() +OH-
+OH-![]() NH3·H2O
NH3·H2O
D. 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质混合后,不能生成NaOH的是 ( )
A. Na和H2O B. Na2O2和H2O
C. Ca(OH)2溶液和Na2CO3溶液 D. Ca(OH)2溶液和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组同学查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为Ca(ClO)2+CaCl2+2H2SO4 ![]() 2CaSO4+2Cl2↑+2H2O,他们设计了如图1所示的制取氯气并验证其性质的实验装置:
2CaSO4+2Cl2↑+2H2O,他们设计了如图1所示的制取氯气并验证其性质的实验装置: 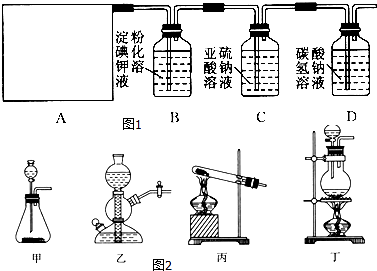
请回答下列问题:
(1)该实验中A部分的装置是图2中的 .
(2)A中发生反应一段时间后,B中的现象是 . B中发生反应的化学方程式为 .
整套实验装置存在的明显缺陷是 .
(3)写出D装置中发生反应的离子方程式 .
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的Na2SO3已被氧化为Na2SO4(简述实验步骤): .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
以芳香烃A为原料合成有机物F和I的合成路线如下: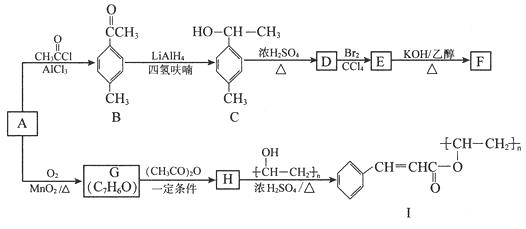
(1)A的分子式为 , C中官能团名称为。
(2)D分子中最多有个原子共平面。
(3)E生成F的反应类型为 , G的结构简式为。
(4)由H生成I的化学方程式为。
(5)符合下列条件的B的同分异构体有种(不考虑立体异构),其中核磁共振氢谱为4组峰且面积比为6∶2∶1∶1的是
(写出其中一种的结构简式)。
①属于芳香化合物 ②能发生银镜反应
(6)已知RCOOH ![]() RCOCl,参照上述合成路线,以苯和丙酸为原料(无机试剂任选),设计制备
RCOCl,参照上述合成路线,以苯和丙酸为原料(无机试剂任选),设计制备 ![]() 的合成路线。
的合成路线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com