
【题目】在一定条件下,当加入80 g SO2气体发生催化氧化反应生成SO3气体时,放出热量98.3 kJ,已知SO2在此条件下转化率为80%,据此,下列热化学方程式正确的是( )
A. SO2(g)+1/2O2(g)![]() SO3(g) ΔH=-98.3 kJ·mol-1
SO3(g) ΔH=-98.3 kJ·mol-1
B. 2SO2(g)+O2(g)![]() 2SO3(l) ΔH=-196.6 kJ·mol-1
2SO3(l) ΔH=-196.6 kJ·mol-1
C. SO2(g)+1/2O2(g)![]() SO3(g) ΔH=-78.64 kJ·mol-1
SO3(g) ΔH=-78.64 kJ·mol-1
D. 2SO2(g)+O2(g)![]() 2SO3(g) ΔH=196.6 kJ·mol-1
2SO3(g) ΔH=196.6 kJ·mol-1
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】I .合成氨工业在现代农业、国防工业中,有着重要的地位
己知:N2 (g) +3H2 (g) ![]() 2NH3 (g) △H=-92 kJ·mol-1
2NH3 (g) △H=-92 kJ·mol-1
(1)下列有关该反应速率的叙述,正确的是(选填序号)____________。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,但可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量—定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)对于合成氨反应而言,如图有关图象一定正确的是(选填序号) ______________。

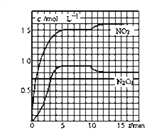
II.向2L的密闭容器中充入7.6molNO和3.8mol O2,发生如下反应:
①2NO(g) + O2(g) =2NO2 (g) ②2NO2 (g) ==N2O4 (g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。
(1)计算前5min N2O4反应的平均速率为________________________。
(2)计算T1℃时反应②的化学平衡常数为_______________________。
(3)若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,判断T1℃时反应②进行的方向_____(正向、逆向、不移动),并计算达到平衡时N2O4的物质的量为_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向恒温恒容密闭容器中充入气体A,发生反应:xA(g)![]() yB(g)+zC(g),各物质的浓度随时间的变化如下表所示。
yB(g)+zC(g),各物质的浓度随时间的变化如下表所示。
时间/s | c(A)/mol L-1 | c(B)/mol L-1 | c(C)/mol L-1 |
0 | 0.540 | 0 | 0 |
5 | 0.530 | 0.015 | 0.020 |
15 | 0.514 | 0.039 | 0.052 |
30 | 0.496 | 0.066 | 0.088 |
下列说法正确的是
A. x+y=3
B. 若起始时在容器中通入氦气,使容器压强增大,各物质反应速率均加快
C. 随着反应的进行,A的反应速率不断减慢,是因为该反应是吸热反应
D. 0~30 s内B的平均生成速率为2.2×10-3 mol L-1 S-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有5种物质: ①甲烷 ②苯 ③聚乙烯 ④1,3-丁二烯 ⑤2-丁炔 其中能使酸性高锰酸钾溶液褪色的是( )
A.① ②B.④ ⑤C.③ ④D.③ ⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是
A. pH=6.5的溶液一定显酸性
B. 0.1mol L-1的Na2CO3溶液中:c(CO32-)+c(HCO3-)=0.1mol L-1
C. 常温下,等体积的0.2 mol L-1的盐酸与0.2 mol L-1的氢氧化钡溶液混合,所得溶液的pH=13
D. 常温下,某溶液中水电离出的c(OH-)=l×10-12 mol L-1,该溶液pH 一定等于2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧气可发生如下反应:P4+5O2===P4O10。已知断裂下列化学键需要吸收的能量分别为P-P:a kJ·mol-1、P—O:b kJ·mol-1、P===O:c kJ·mol-1、O===O:d kJ·mol-1。根据下图所示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )

A. (6a+5d-4c-12b) kJ·mol-1
B. (4c+12b-6a-5d) kJ·mol-1
C. (4c+12b-4a-5d) kJ·mol-1
D. (4a+5d-4c-12b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北京奥运会“祥云”火炬使用的燃料为丙烷。下列关于丙烷的说法正确的是( )
A. 分子中的碳原子在一条直线上 B. 其一氯代物只有一种
C. 能使酸性高锰酸钾溶液褪色 D. 结构简式为CH3CH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属晶体的叙述不正确的是
A.常温下,金属单质不都以金属晶体形式存在
B.金属键在一定外力作用下,会因形变而消失
C.钙的熔、沸点高于钾
D.温度越高,金属的导电性越弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10 mL含等浓度的I-和Cl-的溶液中逐滴加入0.1 mol·L-1的AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。下列说法不正确的是( )

A. 该实验可以证明AgI比AgCl更难溶
B. V1= V2-V1
C. 向最终的沉淀中加入Na2S溶液,沉淀变成黑色
D. 加入V2 mL AgNO3溶液后,溶液中不含I-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com