
【题目】Ⅰ.某实验小组为探究ClO-、I2、SO![]() 在酸性条件下的氧化性强弱,设计实验如下:
在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:__________________________。
(2)实验②的化学反应中转移电子的物质的量是___________________。
(3)以上实验说明,在酸性条件下ClO-、I2、SO![]() 的氧化性由弱到强的顺序是________________。
的氧化性由弱到强的顺序是________________。
Ⅱ.(4)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________(填序号)。
A.Cl2 B.H2O2
C.ClO2 D.O3
(5)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是_______________________(用离子方程式表示)。
【答案】 ClO-+2I-+2H+===I2+Cl-+H2O 0.004 mol SO![]() <I2<ClO- C ClO-+Cl-+2H+===Cl2↑+H2O
<I2<ClO- C ClO-+Cl-+2H+===Cl2↑+H2O
【解析】Ⅰ.(1)实验①说明酸性条件下,次氯酸钠把碘离子氧化生成碘单质,同时自身被还原生成氯离子,该反应中,次氯酸根离子得电子作氧化剂,碘离子失电子是还原剂,氧化产物是碘,所以氧化性强弱为:ClO->I2,反应离子方程式为:ClO-+2I-+2H+=I2+Cl-+H2O,故答案为:ClO-+2I-+2H+=I2+Cl-+H2O;(2)实验②说明碘单质把亚硫酸根离子氧化生成硫酸根离子,自身被还原生成碘离子,氧化剂是碘,还原剂是亚硫酸钠,氧化产物是硫酸根离子,所以氧化性强弱为:I2>SO42-,反应离子方程式为:H2O+I2+SO32-=SO42-+2I-+2H+,设转移电子的物质的量为x.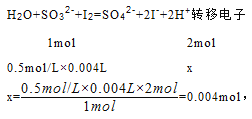
答:转移电子的物质的量是0.004mol;
(3)实验①说明氧化性强弱为:ClO->I2,实验②说明氧化性强弱为:I2>SO42-,所以在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是SO42-、I2、ClO-,故答案为:SO42-、I2、ClO-.
Ⅱ.(4)1mol Cl2(发生的反应为Cl2+H2O=HCl+HClO)、H2O2、ClO2、O3分别消毒时,转移电子依次为1mol、1mol、5mol、2mol,等物质的量的上述物质反应,ClO2转移的电子数最多,消毒效率最高,故答案为:C;(5)ClO-与浓盐酸中的Cl-会发生反应生成有毒的Cl2,方程式为ClO-+Cl-+2H+═Cl2↑+H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】实验室里需480mL1.0mol/LNaOH溶液,若用固体NaOH配制,则应选择的容量瓶规格为
A. 480mL B. 1000mL C. 100mL D. 500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铋酸钠(NaBiNO3)检验溶液中的Mn2+,反应方程式为:4MnSO4+10NaBiO3+14H2SO4═4NaMnO4+5Bi2(SO4)3+3Na2SO4+口,下列说法不正确的是
A. 口内的物质为水,配平系数为14。
B. 若生成1mol NaMnO4,则转移5mole-
C. 反应方程式中的硫酸可换为盐酸
D. 溶液中有Mn2+的现象是溶液变为紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如下能量关系示意图,下列说法正确的是

A. 1 mol C(g)与1 mol O2(g)的能量之和为393.5 kJ
B. 反应2CO(g)+O2(g) ==2CO2(g)中,生成物的总能量大于反应物的总能量
C. 由C→CO的热化学方程式为:2C(s)+O2(g) ==2CO(g) ΔH= 221.2 kJmol1
D. 热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH= 10.1 kJmol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体可能含有NH4+、Cu2+、Na+、Cl-、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况)。
下列说法正确的是
A. 该固体中一定含有NH4+、CO32-、SO42-、Na+ B. 该固体中一定没有Cu2+、Cl-、Na+
C. 该固体中只含有NH4+、CO32-、SO42-、Cl- D. 根据以上实验,无法确定该固体中有Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化六氨合钴(Ⅲ)是一种重要的化工产品,实验中采用H2O2作氧化剂,在大量氨和氯化铵存在下,选择活性炭作为催化剂将Co(Ⅱ)氧化为Co(Ⅲ),来制备三氯化六氨合钴(Ⅲ)配合物,反应式为:2(CoCl2·6H2O)+10NH3+2NH4Cl+H2O2![]() 2[Co(NH3)6]Cl3+14H2O
2[Co(NH3)6]Cl3+14H2O

已知:①Co(NH3)6Cl3在不同温度下水中的溶解度曲线如图。
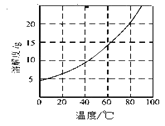
②制备过程中可能用到的部分装置如下:
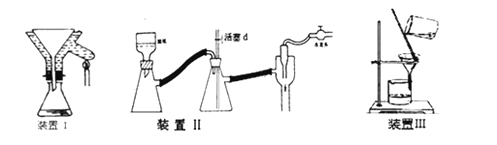
(1)原料NH4Cl的主要作用是_________;步骤④中要冷却至10℃再加入H2O2溶液,这样操作的目的:_____。
(2)步骤⑤中保持60℃的加热方法是_____,恒温20分钟的目的是_____。
(3)步骤⑥是减压抽滤(见上图装置Ⅱ),当抽滤完毕或中途停止抽滤时,防自来水倒吸入抽滤瓶最佳的正确操作是_____。
(4)操作A的名称为_____。若操作过程中,发现漏斗尖嘴处有少量晶体析出,处理方法是_________。
(5)步骤⑨进行洗涤时要用到两种试剂,应该依次用_____(填序号)洗涤。
A. 饱和氯化钠溶液 B. 无水乙醇 C. 浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的分类、名称(或俗名)、化学式中不能完全对应的是( )
A.碱性氧化物、过氧化钠、Na2O2
B.酸性氧化物、三氧化硫、SO3
C.正盐、苏打、Na2CO3
D.含氧酸、次氯酸、HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关表述正确的是
(1)乙烯使酸性高锰酸钾溶液褪色发生的是氧化反应
(2)石油的分馏和煤的干馏都是物理变化
(3)Fe2+的离子结构示意图:
(4)CO2的比例模型图:![]()
(5)丙烷的分子球棍模型图:
A. (1)(2) B. (2)(4) C. (1)(5) D. (1)(3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com