
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF,下列有关该反应的说法正确的是
A. NF3是氧化剂,H2O是还原剂
B.若生成1 mol HNO3,则转移2mol电子
C.还原剂和氧化剂的物质的量之比是2:1
D.每消耗0. 2 mol氧化剂,可收集到5.418L气体
【知识点】氧化还原反应B3B4
【答案解析】B 解析:A、只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,故A错误; B、生成1molHNO3,转移的电子的物质的量为1mol×(5-3)=2mol,故B正确;C、NF3生成NO,被还原,做氧化剂,NF3生成HNO3,被氧化,做还原剂,还原剂与氧化剂的物质的量之比为1:2 ,故C错误;D、每消耗0. 2 mol氧化剂,可收集0.2molNO,0.9molHF,共1.1mol,标况下体积为24.64L,,故D错误;
故答案选B
【思路点拨】本题考查氧化还原反应,题目难度中等,注意化合价的升降为氧化还原反应的特征,注意从化合价的角度分析。


科目:高中化学 来源: 题型:
在t℃时,某NaOH稀溶液中,c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=13,则在该温度下,将100 mL 0.10 mol/L的稀硫酸与100 mL 0.40 mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)( )
A.11.52 B.11.70
C.11.82 D.12.00
查看答案和解析>>
科目:高中化学 来源: 题型:
元素及其化合物丰富了物质世界,下列说法正确的是( )
A.铜在冷的浓硫酸中会钝化,所以把铜放入冷的浓硫酸中无明显现象
B.NaOH溶液和AlCl3溶液相互滴加的现象不同
C.金属比非金属易失电子,所以金属可以置换非金属,而非金属不能置换金属
D.Al与热水反应困难,故活泼性不及Al的金属在任何条件下均不能与H2O发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某pH=1的X溶液中可能含有Fe2+、A13+、NH4+、CO32―、SO32―、SO42―、C1―中的若干种,现取X溶 液进行连续实验,实验过程及产物如下:
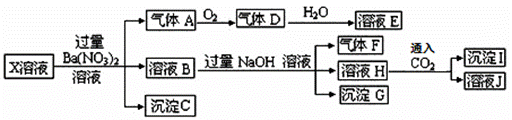
下列说法正确的是( )
A.气体A是NO2
B.X中肯定存在Fe2+、A13+、NH4+、SO42―
C.溶液E和气体F不能发生化学反应
D.X中不能确定的离子是 A13+和C1―
查看答案和解析>>
科目:高中化学 来源: 题型:
对溴甲苯是合成农药溴螨酯的重要原料。工业用液溴、甲苯与1-丙醇共热合成对溴甲苯和1-溴丙烷,其原子利用率很高。实验室模拟的合成流程和相关数据如下:已知:甲苯与溴在有水存在时能反应。
| 物质 | 甲苯 | 1-丙醇 | 1-溴丙烷 |
| 沸点℃ | 110.8 | 97.2 | 71 |
| 物质 | 对溴甲苯 | 邻溴甲苯 | |
| 沸点℃ | 184.3 | 181.7 |
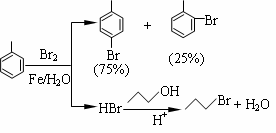
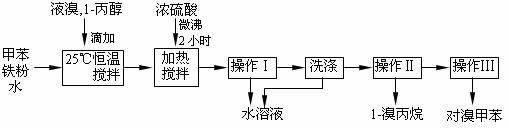
(1)液溴的颜色是__ __ __,实验室存放液溴时应密闭保存,同时需要在试剂瓶中加__ ___,以减少挥发。
(2)25℃恒温搅拌至溴的颜色完全褪去时完成甲苯的溴代反应。搅拌的目的是__________。加入水的作用是:易于控制温度;____________________。
(3)加热搅拌操作中加入浓硫酸,搅拌,完成1-丙醇的取代反应,加入浓硫酸的作用是___ ___,加热微沸2小时的目的是_______ _____。
(4)操作Ⅰ的名称是___________,洗涤操作应在_________(填写仪器名称)中进行。
(5)经以上分离操作后,粗对溴甲苯中还含有的最主要杂质为________(填写名称),使用操作Ⅱ分离出1-溴丙烷的原理是______________________________________。
(6)分离出的水溶液中含HBr、H2SO4和Fe3+离子,将水溶液稀释定容至1000mL,取20.00mL,加入几滴甲基橙作指示剂,用一定浓度的NaOH溶液滴定,测定出HBr的物质的量明显低于理论值,原因是_____________________;有同学认为无需加入指示剂,也能完成滴定,提出这一观点的理由是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
葡萄酒常用Na2S2O5作抗氧化剂。中华人民共和国国家标准(G112760-2011)规定葡萄酒中抗氧化剂的残留量(以游离SO2计算)不能超过0.25g/L。某兴趣小组用下图装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
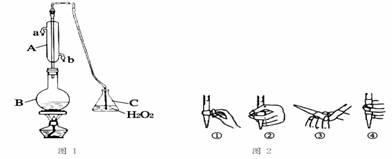
(1)仪器A的名称是 。水通入A的进口为 (填字母)。
(2)B中加人300. 00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应.其化学方程式为 。
(3)除去C中过量的H2O2,然后用0.0900 mol/L NaOH标准溶液进行滴定,滴定前排气泡时,应选择上述图2中的 (填序号);若滴定终点时溶液的pH=8.8,则选择的指示剂为 ;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积 (填序号)(①= 10mL;②=40mL; ③<10mL;④>40mL)
(4)配制100 mL 0. 0900 mol/LNaOH标准溶液的操作如下:
①烧杯中的溶液冷却到室温后,小心转入仪器X中
②将用托盘天平称量好的NaOH固体放入小烧杯中,加适量蒸馏水溶解
③继续加蒸馏水至液面离刻度线1~2 c m处,改用胶头滴管小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液都小心转入仪器X中,并轻轻摇匀
⑤将仪器X塞紧,充分摇匀。
上述操作步骤的正确顺序为 (填序号)。仪器X的名称是 。
(5)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为 g/L。
(6)该测定结果比实际值偏高.可能的原因是 ,利用现有装置提出改进的措施为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或原理不正确的是( )
|
| A. | 纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
|
| B. | 分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒 |
|
| C. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
|
| D. | 测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,与对应的标准比色卡比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中物质的量浓度为1mol/L的是( )
|
| A. | 将40 g NaOH溶解于1 L水中 |
|
| B. | 将22.4 L HCl气体溶解于水配成1 L溶液 |
|
| C. | 将1 L 5 mol/L的盐酸加水稀释至5L |
|
| D. | 将10 g NaOH配制成 250 mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,可以迅速杀灭多种微生物,包括多种病毒(如SARS病毒)、细菌、真菌及芽孢。过氧乙酸可由冰醋酸与过氧化氢在一定条件下作用制得,下列有关过氧乙酸的叙述中正确的是
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸与苯酚混合使用,可增强过氧乙酸杀菌效果
C.由下列过氧乙酸的制取原理可以看出,过氧乙酸是酯的同系物
O
||
CH3COOH+H—O—O—H—→CH3—C—O—O—H+H2O
D.浓过氧乙酸溶液中加入少许紫色石蕊试液,振荡后先变红,后褪色。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com