
【题目】有转化关系(其他产物及反应所需条件均已略去).
A ![]() B
B ![]() C
C ![]() D
D ![]() E
E ![]() F,以下推断错误的是( )
F,以下推断错误的是( )
A.当X是盐酸时,则F是稀硝酸
B.当X是氢氧化钠时,则F是稀硝酸
C.当X是氢氧化钠时,B跟Cl2反应可能有白烟现象
D.当X是氢氧化钠时,B能使酸性高锰酸钾溶液褪色
【答案】A
【解析】解:A.当X是盐酸时,A是金属或金属氧化物,金属或金属氧化物和酸反应生成盐B,如果盐B能和氯气反应生成C,则C也是盐,且是高价盐,C和氧气不反应,所以不能最后生成硝酸,故A错误;
B.当X是氢氧化钠时,A是铵盐,铵盐和氢氧化钠反应生成氨气B,氨气和氯气反应生成氮气和氯化铵,氮气和氧气反应生成一氧化氮,一氧化氮和氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸,则F是硝酸,符合条件,故B正确;
C.当X是氢氧化钠时,A是铵盐,铵盐和氢氧化钠反应生成氨气B,氨气和氯气反应生成氮气和固体氯化铵,所以有白烟生成,故C正确;
D.当X是氢氧化钠时,A是硫化氢,硫化氢和氢氧化钠反应生成硫化钠,硫化钠和氯气反应生成氯化钠和硫,硫在氧气中燃烧生成二氧化硫,二氧化硫和氧气在一定条件下反应生成三氧化硫,三氧化硫和水反应生成硫酸,硫化氢有还原性,酸性高锰酸钾溶液有强氧化性,所以硫化氢能使高锰酸钾溶液褪色,故D正确;
故选A.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】铊(81T1)是元素周期表ⅢA族元素,下列关于铊的叙述不正确的是( )
A. 铊比铝的金属性更强
B. 铊能与盐酸反应放出氢气
C. 铊在化合物中可以是+3价
D. 氢氧化铊一定具有两性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有转化关系(其他产物及反应所需条件均已略去).
A ![]() B
B ![]() C
C ![]() D
D ![]() E
E ![]() F,以下推断错误的是( )
F,以下推断错误的是( )
A.当X是盐酸时,则F是稀硝酸
B.当X是氢氧化钠时,则F是稀硝酸
C.当X是氢氧化钠时,B跟Cl2反应可能有白烟现象
D.当X是氢氧化钠时,B能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关 ![]() 分子结构的下列叙述中正确的是( ) ①除苯环外的其余碳原子有可能都在一条直线上
分子结构的下列叙述中正确的是( ) ①除苯环外的其余碳原子有可能都在一条直线上
②除苯环外的其余碳原子不可能都在一条直线上
③12个碳原子不可能都在同一平面上
④12个碳原子有可能都在同一平面上.
A.①②
B.②③
C.①③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)NaClO溶液pH>7,用离子方程式表示原因__________
(2)根据NaClO的性质推测,在纸浆中加入NaClO溶液的目的是_________________。
(3)某小组同学用如图所示装置探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。反应的离子方程式_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑两球的浮力变化)( )

A. 杠杆为导体或绝缘体时,均为A端高B端低
B. 杠杆为导体或绝缘体时,均为A端低B端高
C. 当杠杆为导体时,A端低B端高
D. 当杠杆为导体时,A端高B端低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是( )
A.氢氧根离子的电子式是 ![]()
B.二氧化碳分子的比例模型是 ![]()
C.芳香烃的组成通式是CnH2n﹣6(n≥6)
D.12C和14C的原子结构示意图均可表示为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为Mg/mol.若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为 .
(2)该气体在标准状况下的体积为
(3)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 .
(4)该气体溶于水后形成V L溶液,其溶液中溶质的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的化合物与人类生产、生活密切相关.
(1)C、CO、CO2在实际生产中有如下应用:a.2C+SiO2 ![]() Si+2CO b.3CO+Fe2O3
Si+2CO b.3CO+Fe2O3 ![]() 2Fe+3CO2
2Fe+3CO2
c.C+H2O ![]() CO+H2 d.CO2+CH4
CO+H2 d.CO2+CH4 ![]() CH3COOH
CH3COOH
上述反应中,理论原子利用率最高的是 .
(2)有机物加氢反应中镍是常用的催化剂.但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2 , 为搞清该方法对催化剂的影响,查得资料:
则:①不用通入O2氧化的方法除去CO的原因是 .
②SO2(g)+2CO(g)=S(s)+2CO2(g)△H= .
(3)汽车尾气中含大量CO和氮氧化物(NO2)等有毒气体.①活性炭处理NO的反应:C(s)+2NO(g)N2(g)+CO2 (g)△H=﹣akJmol﹣1(a>0)
若使NO更加有效的转化为无毒尾气排放,以下措施理论上可行的是: . 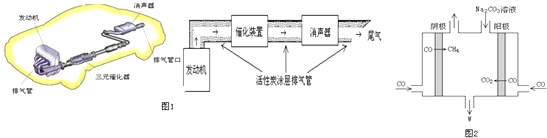
a.增加排气管长度 b.增大尾气排放口
c.添加合适的催化剂 d.升高排气管温度
②在排气管上添加三元催化转化装置,CO能与氮氧化物(NO2)反应生成无毒尾气,其化学方程式是 .
(4)利用CO2与H2反应可合成乙醚.以KOH为电解质溶液,组成乙醚﹣﹣﹣﹣空气燃料电池,该电池工作时其负极反应式是 .
(5)电解CO制备CH4和W,工作原理如图2所示,生成物W是 , 其原理用电解总离子方程式解释是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com