
【题目】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是____________。
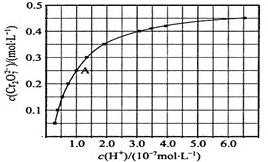
(2)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol·L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
①用离子方程式表示Na2CrO4溶液中的转化反应__________。
②由图可知,溶液酸性增大,CrO42的平衡转化率___________(填“增大“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为___________。
③升高温度,溶液中CrO42的平衡转化率减小,则该反应的ΔH_________0(填“大于”“小于”或“等于”)。
(3)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72还原成Cr3+,反应的离子方程式为_____________。
【答案】开始有灰蓝色沉淀生成,随后沉淀溶解 2CrO42-+2H+![]() Cr2O72-+H2O 增大 1014 小于 5H++Cr2O72-+3HSO3-=2Cr3++3SO42-+4H2O
Cr2O72-+H2O 增大 1014 小于 5H++Cr2O72-+3HSO3-=2Cr3++3SO42-+4H2O
【解析】
(1) Cr2(SO4)3为强电解质,则溶液中存在Cr3+(蓝紫色),加入NaOH溶液时生成Cr(OH)3灰蓝色沉淀,Cr3+与Al3+的化学性质相似,加入过量NaOH时生成Cr(OH)4(绿色);
(2) ①已知CrO42和Cr2O72在溶液中可相互转化,且与c(H+)有关;
②由图可知,溶液酸性增大,溶液中的c(Cr2O72)逐渐增大,则CrO42的平衡转化率增大;;K= c(Cr2O72)/[ c2(Cr2O72)×c2(H+)];
③升高温度,溶液中CrO42的平衡转化率减小,则反应逆向进行,逆向反应为吸热反应;
(3)已知常用NaHSO3将废液中的Cr2O72还原成Cr3+,则+4价的S变为+6价;
(1) Cr2(SO4)3为强电解质,则溶液中存在Cr3+(蓝紫色),加入NaOH溶液时生成Cr(OH)3灰蓝色沉淀,Cr3+与Al3+的化学性质相似,加入过量NaOH时生成Cr(OH)4(绿色),可观察到的现象为:开始有灰蓝色沉淀生成,随后沉淀溶解;
(2) ①已知CrO42和Cr2O72在溶液中可相互转化,且与c(H+)有关,反应的离子反应式为:2CrO42-+2H+![]() Cr2O72-+H2O;
Cr2O72-+H2O;
②由图可知,溶液酸性增大,溶液中的c(Cr2O72)逐渐增大,则CrO42的平衡转化率增大;A点数据为c(H+)=1.0×10-7mol/L,c(Cr2O72)=0.25 mol/L,则c(CrO42)=0.5 mol/L,K= c(Cr2O72)/[ c2(Cr2O72)×c2(H+)]= 1014,答案为:增大;1014;
③升高温度,溶液中CrO42的平衡转化率减小,则反应逆向进行,逆向反应为吸热反应,ΔH小于0,答案为小于;
(3)已知常用NaHSO3将废液中的Cr2O72还原成Cr3+,则+4价的S变为+6价,生成硫酸根离子,反应的离子方程式为:5H++Cr2O72-+3HSO3-==2Cr3++3SO42-+4H2O;


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】如图装置中,观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
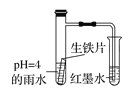
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.具支试管中溶液pH逐渐减小
D.墨水回升时,碳极反应式为O2+2H2O+4e–=4OH–
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用某浓度的NaOH溶液滴定20.00 mL等浓度的CH3COOH溶液,所得滴定曲线如图。下列说法正确的是( )
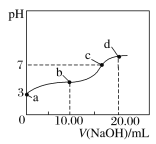
A.c点溶液中c(Na+)∶c(CH3COO-)=1∶1
B.a、b两点对应的醋酸的电离平衡常数:a<b
C.a点醋酸溶液的浓度为1.0×10–3 mol·L–1
D.升高温度,d点溶液pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A.Na(s)![]() Na2O(s)
Na2O(s)![]() NaOH(aq)
NaOH(aq)
B.Al2O3(s)![]() AlCl3(aq)
AlCl3(aq)![]() Al(s)
Al(s)
C.CaSO4(s)![]() CaCO3(s)
CaCO3(s)![]() Ca(NO3)2(aq)
Ca(NO3)2(aq)
D.Fe2O3(s)![]() Fe(s)
Fe(s)![]() Fe2(SO4)3(aq)
Fe2(SO4)3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO﹣)﹣c(Na+)=________(填准确数值)。
(2)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为___________________________________。
(3)写出使用泡沫灭火器时发生反应的离子方程式_________________________________。
(4)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈_______(填“酸性”,“中性”或“碱性”),溶液中c(Na+) _______c(CH3COO-)(填“ >” 或 “=”或“<”)。
(5)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈_______(填“酸性”,“中性”或“碱性”)。
(6)25℃时,体积为Va、pH=a的某一元强酸溶液与体积为Vb、pH=b的某一元强碱溶液均匀混合后,溶液的pH=7,已知b=2a,Va<Vb,则a的取值范围为________。
(7)今有a·盐酸 b·硫酸 c·醋酸三种酸:完全中和含等物质的量的NaOH的溶液,消耗相同pH的上述三种酸溶液的体积由大到小的顺序是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )

A. a和b都属于芳香族化合物
B. a和c分子中所有碳原子均处于同一平面上
C. a、b和c均能使酸性KMnO4溶液褪色
D. b和c均能与新制的Cu(OH)2反应生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是
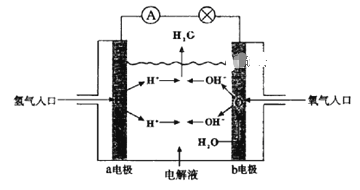
A. a电极是负极
B. 氢氧燃料电池是一种具有应用前景的绿色电源
C. b电极的电极反应为:4OH--4e-=2H2O+O2↑
D. 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. lmol 该有机物( )最多能与4mol 氢气加成
)最多能与4mol 氢气加成
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 乳酸薄荷醇酯( )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
D.  分子中至少有9个碳原子处于同一平面上
分子中至少有9个碳原子处于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从植物组织中获取挥发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的果皮中提取的精油90%以上是柠檬烯(柠檬烯![]() )。提取柠檬烯的实验操作步骤如下:
)。提取柠檬烯的实验操作步骤如下:

①将12个橙子皮剪成细碎的碎片,投入乙装置中,加入约30mL水;
②松开活塞K。加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧,打开冷凝水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。
下列说法不正确的是( )
A.当馏出液无明显油珠,澄清透明时,说明蒸馏完成
B.蒸馏结束后,先把乙中的导气管从溶液中移出,再停止加热
C.为完成实验目的,应将甲中的长导管换成温度计
D.要想从精油中得到柠檬烯,还需要进行萃取、分液、蒸馏操作才能实现目的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com