
【题目】[2016新课标Ⅰ]化学与生活密切相关。下列有关说法错误的是
A.用灼烧的方法可以区分蚕丝和人造纤维
B.食用油反复加热会产生稠环芳烃等有害物质
C.加热能杀死流感病毒是因为蛋白质受热变性
D.医用消毒酒精中乙醇的浓度为95%
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一。请回答下列问题:
(1)Cr元素的基态原子电子排布式为_____________________,比较Fe和Mn的各级电离能后发现,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子______(填“难”或“易”)。
(2)Cu元素处于周期表____________区,向盛有硫酸铜的试管里加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,此时的离子方程式为______________,若加入乙醇将析出____________色的晶体,其配离子的离子构型为_____________
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应)。用A、B、O表示这类特殊晶体的化学式:_____________。
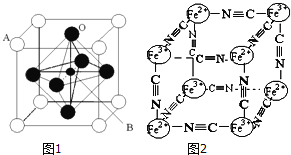
(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如上图的图2所示,该晶体的化学式可表示为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物阿司匹林可由水杨酸制得,它们的结构如图所示。有关说法正确的是( )

A. 1 mol阿司匹林最多可消耗3 molH2
B. 水杨酸分子中所有原子不可能共面
C. 水杨酸可以发生取代、加成、氧化、加聚反应
D. 1 mol阿司匹林最多可消耗2 molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CO2转化为甲醇的原理为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH <0。500 ℃时,在体积为1 L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( )
CH3OH(g)+H2O(g) ΔH <0。500 ℃时,在体积为1 L 的固定容积的密闭容器中充入1mol CO2、3mol H2,测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( )

A.曲线X可以表示CH3OH(g)或H2O(g)的浓度变化
B.从反应开始到10min时,H2的反应速率υ(H2)=0.225 mol/(L·min)
C.平衡时H2 的转化率为75%
D.500 ℃时该反应的平衡常数K=3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在科学研究和工业生产中具有许多用途。请回答下列问题:
(1)画出基态Cu原子的价电子排布图_______________;
(2)已知高温下Cu2O比CuO稳定,从核外电子排布角度解释高温下Cu2O更稳定的原因____________________________________;
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是___________,配体中提供孤对电子的原子是________。C、N、O三元素的第一电离能由大到小的顺序是_______________(用元素符号表示)。
(4)铜晶体中铜原子的堆积方式如图1所示,则晶体铜原子的堆积方式为____________。

(5)M原子的价电子排布式为3s23p5,铜与M形成化合物的晶胞如图2所示(黑点代表铜原子)。
①该晶体的化学式为_____________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于________化合物(填“离子”、“共价”)。
③已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,已知该晶体中Cu原子和M原子之间的最短距离为体对角线的1/4,则该晶体中Cu原子和M原子之间的最短距离为___________pm(写出计算列式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将一定量的A、B、C三种物质(都是气体)放入固定体积为10 L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如下图所示。
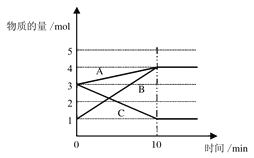
请解答下列问题:
①该反应的的反应物是_______(填字母),生成物是________(填字母),反应的化学方程式用A、B、C可表示为____________________________(用字母表示)
②用B的浓度变化表示在0~10 min内的反应速率是__________
③判断该反应达到化学平衡状态的标志是___________(填字母)
a.A和B浓度相等 b.A百分含量保持不变
c.A的生成速率与B的消耗速率相等 d.容器中气体的压强不变
e.容器中混合气体的密度保持不变
(2)由铜、锌和稀硫酸组成的原电池中,正极是_______(填化学式),发生_______反应,电极反应是________________________;负极是_______(填化学式),发生________反应,总的反应式(离子方程式)是______________________。
(3)从能量的角度看,断开化学键要______能量(填吸收或放出,下同),形成化学键要_____能量。当反应物的总能量高于生成物时,该反应为_______反应(填吸热或放热,下同);当反应物的总能量低于生成物时,该反应为__________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存的无色透明离子组是( )
A.K+、Na+、NO3-、MnO4- B.K+、Na+、Cl-、SO42-
C.K+、Na+、Br-、Cu2+ D.Na+、Ba2+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期元素的原子序数依次增大。A和C,B和E同主族,C、D、E同周期。由A、B组成的两种化合物甲和乙都为液态,甲中A、B原子数之比为2:1,乙中为1:1。由B、C组成的两种化合物丙和丁都为固态,丙中C、B原子数之比为2:1,丁中为1:1。C、D、E的最高价氧化物对应的水化物两两之间均能发生反应,且均有甲生成,且A为原子半径最小的短周期元素,丁为淡黄色固体。则:
(1)D的原子结构示意图为:__________________
(2)A元素的单质为:_____________(填化学式);丁的电子式为:_____________
(3)E在周期表中的位置_________________________________
(4)C、D的最高价氧化物对应水化物发生反应的离子方程式为:
____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰元素广泛分布在自然界中,其单质和化合物在工农业生产中有着重要的应用。
(1)已知相关热化学方程式为:
4Al(s)+3O2(g)=2Al2O2(s) △H1=a kJmol﹣1
3MnO2(s)=Mn3O4(s)+O2(g) △H2=bkJmol﹣1
3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) △H3=ckJmol﹣1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) △H=__ kJmol﹣1(用含a、b、c的代数式表示).
(2)MnCO3广泛用作锰盐原料.通过如图装置焙烧MnCO3可以制取MnO2,反应方程式为:2MnCO3(s)+O2(g)═2MnO2(s)+2CO2(g)。
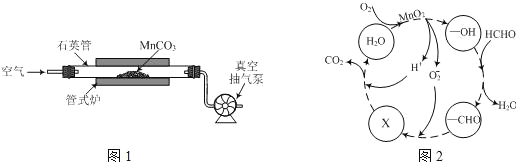
①2MnCO3(s)+O2(g)2MnO2(s)+2CO2(g)的化学平衡常数表达式K=______。
②用真空抽气泵不断抽气的目的除保证反应持续进行外,还有______。
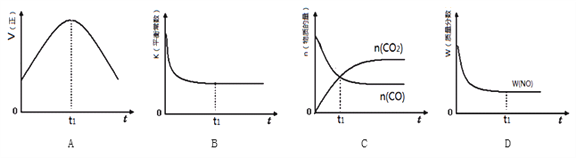
③若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填序号)。(如图中V正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
(3)MnO2常用作催化剂。MnO2催化降解甲醛的反应机理如图所示,图中X表示的粒子是______,该反应的总反应方程式为______。
(4)MnSO4是重要微量元素肥料。用惰性电极电解MnSO4溶液可以制得更好活性的MnO2,电解时总反应的离子方程式为:______,电解过程中阴极附近的pH______(选填“增大”、“减小”或“不变”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com