
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是( )

A.电流由O2所在的铂电极流出
B.该电池的负极反应式为:CH3CH2OH+3H2O+12e-═2CO2↑+12H+
C.O2所在的铂电极处发生还原反应
D.微处理器通过检测电流大小而计算出被测气体中酒精的含量
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】水的电离过程为H2OH++OH-,在不同温度下其离子积为Kw(25℃)=1.0×10-14,Kw(35℃)=2.1×10-14,则下列叙述中正确的是( )
A.c(H+)随温度的升高而降低
B.35℃时,c(H+)>c(OH-)
C.溶液pH:pH(35℃)>pH(25℃)
D.35℃时已电离的水的浓度约为1.45×10-7mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10 mL 0.1 mol/LCuCl2溶液中滴加0.1 mol/L的Na2S溶液,滴加过程中溶液中lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知:lg2=0.3,Ksp(ZnS)=3×10-25 。下列有关说法正确的是( )

A.a、b、c三点中,水的电离程度最大的为b点
B.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+)
C.该温度下Ksp(CuS)=4×10-36
D.向100 mL Zn2+、Cu2+浓度均为10-5 mol/L的混合溶液中逐滴加入10-4 mol/L的Na2S溶液,Zn2+先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如下图装置。下列叙述不正确的是
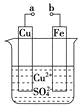
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C.a和b用导线连接时,电子由铜电极流向铁电极
D.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作与现象、结论都正确且有相关性的是
选项 | 操作 | 现象 | 结论 |
A |
|
| 原溶液中仍有 |
B | 向含有ZnS和 | 生成黑色沉淀 |
|
C | 向 | 溶液变浑浊 | 酸性 |
D | 向乙酸乙酯粗产品中加入少量 | 产生大量气泡 | 乙酸乙酯产品中混有乙醇 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种有机物分别由碳、氢、氧元素中的两种或三种元素组成各取四种有机物0.1mol,分别完全燃烧,均能得到4.48 L(标准状况下)二氧化碳,D的水溶液显酸性。四种有机物转化关系如图:
![]()
回答下列问题:
(1)A、D分子中所含官能团的名称分别是______、______。
(2)a mol A、B的混合气体完全燃烧,消耗氧气的体积为______(标准状况)。
(3)B→C的化学方程式________,反应类型______。
(4)在实验室里可以用如图所示的装置制取乙酸乙酯。
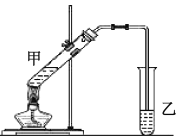
①写出用![]() 与乙酸发生酯化反应的化学方程式_________。
与乙酸发生酯化反应的化学方程式_________。
②反应开始前,试管乙中盛放的试剂为______,制乙酸乙酯时,试管甲中试剂加入顺序为______。
③合成乙酸乙酯的反应为放热反应,实验表明,反应温度应控制在85℃左右为宜。本实验温度不宜低于85℃左右的原因是________。
(5)对所得乙酸乙酯粗产品的提纯过程如下(已知:氯化钙与乙醇生成难溶物)。
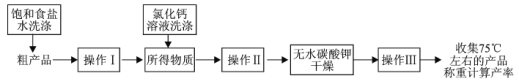
图中操作Ⅰ的名称为_______,操作Ⅱ的名称为_______,操作Ⅲ的名称为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答下列问题:

(1)B极是电源的___;一段时间后,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明___,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为___。
(3)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是___。
(4)现用丙装置给铜件镀银,则H应该是__(填“镀层金属”或“镀件”)。当乙中溶液的pH是13时(乙溶液体积为500mL,不考虑反应过程溶液体积变化),丙中镀件上析出银的质量为__g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.强碱性溶液中NaClO将Fe(OH)3氧化为FeO42-:3ClO+2Fe(OH)3=2FeO42-+3Cl+4H++H2O
B.硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
C.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:S2O32-+2H+=SO2↑+S↓+H2O
D.向NH4HCO3溶液中加入足量石灰水:Ca2++HCO3-+OH=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c)表示止水夹。

请按要求填空:(可供选择的试剂有:Cu片,MnO2粉末,浓硝酸,稀硝酸,浓硫酸,浓盐酸,氢氧化钠溶液,酚酞)
(1)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。若在丙中加入适量水,即可制得氯水。将所得氯水加入到滴有酚酞的NaOH溶液中,观察到溶液褪色,甲同学给出的结论是氯水溶于水生成了酸,将NaOH中和后溶液褪色。
a.写出制取氯气的化学方程式:___。
b.乙同学认为甲同学的结论不正确,他认为褪色的原因可能是___。
c.如何验证甲、乙两同学的结论(写出所加试剂,现象,结论):___。
(2)B、D、E装置相连后,可制得NO2并进行有关实验。
①B中发生反应的化学方程式为___。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹___,再打开止水夹___,使烧杯中的水进入试管丁的操作是___。
③试管丁中的NO2与水充分反应,若向试管内缓缓通入一定量的O2,直到试管全部充满水,则所得溶液中的溶质的物质的量浓度是___(气体按标准状况计算,结果保留二位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com