
【题目】将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( ) 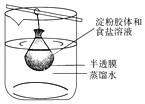
A.烧杯内液体加入硝酸银溶液后有白色沉淀产生
B.烧杯内液体加入碘水后呈蓝色
C.袋内液体加入硝酸银溶液后不会出现白色沉淀
D.袋内液体加入碘水后不变蓝
【答案】AC
【解析】解:淀粉胶体和氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中后,淀粉胶体不能通过半透膜而留在袋内,但是氯离子和钠离子能通过半透膜而进入烧杯的水中.
A.烧杯内液体含有钠离子和氯离子,加入硝酸银有白色沉淀,故A正确;
B.烧杯内液体含有钠离子和氯离子,不含有淀粉,加入碘水后无现象,故B错误;
C.袋内液体不含氯离子,加入硝酸银溶液后不会出现白色沉淀,故C正确;
D.袋内液体含有淀粉,加入碘水变蓝,故D错误;
故选:AC.
【考点精析】根据题目的已知条件,利用胶体的重要性质的相关知识可以得到问题的答案,需要掌握胶体的性质:①丁达尔现象(可用来鉴别胶体和溶液) ②布朗运动 ③电泳现象 ④胶体聚沉(加入电解质、加入带异种电荷的胶体、加热,均可使胶体聚沉).


科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛。在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下表:
温度/℃ | 200 | 300 | 400 | 500 | 600 |
氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
请回答:
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是_______。
(2)在一定温度下,将2molN2和6molH2通入到体积为2L的密闭容器中,发生反应N2+3H2![]() 2NH3,2min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=_______________(结果用最简分数表示);欲使K增大,可以采取的措施是______。
2NH3,2min达到平衡状态时,H2转化率是50%,该温度下的平衡常数K=_______________(结果用最简分数表示);欲使K增大,可以采取的措施是______。
(3)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是______(选填序号字母)
a.及时分离出NH3 b.升高温度 c.增大压强 d.使用催化剂
(4)NH3能分解为N2和H2,在相同条件下,测得分解后混合气体密度为分解前的2/3,则氨的分解率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,1体积水溶解700体积氨气,所得溶液密度为0.9gcm﹣3 , 这种氨水的物质的量浓度和溶质的质量分数分别为( )
A.18.4molL﹣1 34.7%
B.20.4molL﹣1 38.5%
C.18.4molL﹣1 38.5%
D.20.4molL﹣1 34.7%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中加入稀硫酸,能产生使澄清石灰水变浑浊的无色无味的气体;再加入氯化钡溶液,能产生白色沉淀。关于该溶液的下列结论中正确的是( )
A. 一定含有碳酸根离子 B. 一定含有碳酸氢根离子
C. 一定含有硫酸根离子 D. 可能含有硫酸根离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列说法正确的是( )
A. 标况下,11.2L CO2中含有氧原子数为2NA
B. 常温下,0.9g H2O中,含有的电子数为0.5NA
C. 标准状况下,2.24L CCl4所含的原子数为0.5NA
D. 1molL-1的Na2SO4溶液中,含Na+的个数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1~100 nm(纳米)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的分散系
① 是溶液 ② 是胶体 ③ 能产生丁达尔效应 ④ 能透过滤纸 ⑤ 不能透过滤纸 ⑥ 静置后会析出黑色沉淀
A.①④⑥ B.②③④ C.②③⑤ D.①③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下二氯化二硫(S2 Cl2)为红棕色液体,其结构式为Cl-S-S-Cl。其制备反应及与水反应的化学方程式如下:①CS2+3Cl2![]() CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2↑+3S↓,则下列说法正确的是
CCl4+S2Cl2 ②2S2Cl2+2H2O=4HCl+SO2↑+3S↓,则下列说法正确的是
A. 反应①中CS2作氧化剂
B. 反应①中每生成1mol S2Cl2转移4mol电子
C. 反应②中氧化产物与还原产物的物质的量之比为3:1
D. 反应②中S2Cl2既作氧化剂又作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将224.00L氯化氢气体溶于635.00mL的水(密度为1.00g/cm3)中,所得盐酸的密度为1.18g/cm3 . (要求有解题过程)
(1)该盐酸的质量分数是多少?
(2)取这种盐酸100.00mL,稀释到500.00mL,所得的稀盐酸的物质的量浓度为多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com