
【题目】NA为阿伏伽德罗常数,下列说法正确的是( )
A. 标况下,11.2L CO2中含有氧原子数为2NA
B. 常温下,0.9g H2O中,含有的电子数为0.5NA
C. 标准状况下,2.24L CCl4所含的原子数为0.5NA
D. 1molL-1的Na2SO4溶液中,含Na+的个数为2NA
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】中和热的测定实验中取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
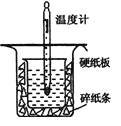
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是__________,除此之外,装置中的一个明显错误是_____________。
(2)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1 NaOH溶液进行反应与上述实验相比,所放出的热量_______(填“相等”或“不相等”)
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(3)近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),通过以上数据计算中和热ΔH=_______( 结果保留小数点后一位)。
(4)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的应用与性质相对应的说法正确的有( )
①光导纤维可用作通讯材料是因为其具有导电性
②明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
③浓硫酸可用作干燥剂是因为其具有脱水性
④MgO、Al2O3的熔点很高,可制作耐高温材料
⑤氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜
⑥NaHCO3能与碱反应,因此食品工业上可用作焙制糕点的膨松剂
⑦A1具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
A. 5个 B. 4个 C. 3个 D. 2个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示)2min后,分别取袋内和烧杯内液体进行实验.下列说法正确的是( ) 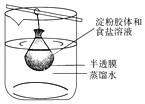
A.烧杯内液体加入硝酸银溶液后有白色沉淀产生
B.烧杯内液体加入碘水后呈蓝色
C.袋内液体加入硝酸银溶液后不会出现白色沉淀
D.袋内液体加入碘水后不变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A. 高纯硅是制造光纤的基本原料
B. 水玻璃是制备硅胶和木材防火剂的原料
C. 活泼金属着火必须用干燥沙土灭火
D. 铝制餐具不宜用来长时间存放咸的食物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.标准状况下,22.4L水中所含的分子数约为6.02×1023
B.标准状况下,aL的氧气和氮气的混合物含有的分子数约为 ![]() ×6.02×1023
×6.02×1023
C.常温常压下,48g O3气体含有的氧原子数为6.02×1023
D.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.2H2S+SO2=3S+2H2O中,氧化产物和还原产物物质的量之比为2:1
B.4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O中,氧化剂和还原剂物质的量之比为5:2
C.3I2+6KOH ![]() 5KI+KIO3+3H2O中,被氧化和被还原的碘元素物质的量之比为1:5
5KI+KIO3+3H2O中,被氧化和被还原的碘元素物质的量之比为1:5
D.2FeS+6H2SO4(浓) ![]() Fe2(SO4)3+3SO2+2S↓+6H2O中,反应中发生氧化反应和发生还原反应的硫元素物质的量之比为2:3
Fe2(SO4)3+3SO2+2S↓+6H2O中,反应中发生氧化反应和发生还原反应的硫元素物质的量之比为2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度(t℃)时,水的离子积为KW=1.0×10﹣13mol2L﹣2,则该温度(填“大于”、“小于”或“等于”)_____25℃,其理由是________________________________。
(2)若将此温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计). 若所得混合液为中性,则a:b=_____;此溶液中各种离子的浓度由大到小排列顺序是_________________。
(3)FeCl3的水溶液呈酸性的原因是(用离子方程式表示):______________。
(4)实验室在配制FeCl3的溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水稀释到所需的浓度,以__ (填“促进”、“抑制”)其水解。
(5)把氯化铝溶液蒸干并灼烧固体产物是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com