
| A、碱性:NaOH<Mg(OH)2<Al(OH)3 |
| B、氢化物稳定性:HF>HCl>PH3 |
| C、原子半径:S>F>O |
| D、酸性:HClO>HNO3>H2CO3 |


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氯气与过量的铁完全反应,转移电子数为2nA |
| B、42gC3H6中含有的共用电子对数目为8nA |
| C、加热下,1molH2和1molI2混合反应生成的气体分子数为2nA |
| D、0.01mol?L-1的KAl(SO4)2溶液中含有0.02nA个SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
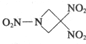
| A、分子中N、O间形成的共价键是非极性键 |
| B、该物质既有氧化性又有还原性 |
| C、C、N、O的第一电离能从大到小的顺序为O>N>C |
| D、C、N、0的气态氢化物的沸点依次降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 人类利用太阳能已有3000多年的历史,太阳能科技突飞猛进.塑晶学名为新戊二醇(NPG),它和液晶相似,塑晶在恒温44℃时,白天吸收太阳能而贮存热能,晚上则放出白天贮存的热能.NPG是一种白色结晶固体,熔点124-130℃,沸点210℃,主要作为生产聚酯树脂、无油醇酸树脂等.已知:NPG的结构式如图,试回答下列问题:
人类利用太阳能已有3000多年的历史,太阳能科技突飞猛进.塑晶学名为新戊二醇(NPG),它和液晶相似,塑晶在恒温44℃时,白天吸收太阳能而贮存热能,晚上则放出白天贮存的热能.NPG是一种白色结晶固体,熔点124-130℃,沸点210℃,主要作为生产聚酯树脂、无油醇酸树脂等.已知:NPG的结构式如图,试回答下列问题: )的二元醇结构可能有:
)的二元醇结构可能有: ,
, ,是一种纤维类织品的阻燃剂,文献记载二溴新戊二醇的合成方法,“季戊四醇先与浓度在98%以上的醋酸进行酯化反应,再通入溴化氢气体进行取代反应,保温后分离出二溴新戊二醇的二酯化物,然后于0.4-0.6Mpa压力下用甲醇和无机酸进行恒压酯分解,该合成方法反应温度低,生成的粗品二溴新戊二醇含量可达88%左右,产品收率高.”试补充合成路线(只写相关反应物和相关生成物)
,是一种纤维类织品的阻燃剂,文献记载二溴新戊二醇的合成方法,“季戊四醇先与浓度在98%以上的醋酸进行酯化反应,再通入溴化氢气体进行取代反应,保温后分离出二溴新戊二醇的二酯化物,然后于0.4-0.6Mpa压力下用甲醇和无机酸进行恒压酯分解,该合成方法反应温度低,生成的粗品二溴新戊二醇含量可达88%左右,产品收率高.”试补充合成路线(只写相关反应物和相关生成物)
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com