
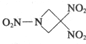
| A、分子中N、O间形成的共价键是非极性键 |
| B、该物质既有氧化性又有还原性 |
| C、C、N、O的第一电离能从大到小的顺序为O>N>C |
| D、C、N、0的气态氢化物的沸点依次降低 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、与生铁相比纯铁更容易被腐蚀 |
| C、金属的吸氧腐蚀和析氢腐蚀都属于电化学腐蚀 |
| D、金属腐蚀的本质是M-ne?=Mn+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 5 |
| 4 |
| 1 |
| 4 |
| A、P4(白磷,s)=4P(红磷,s)△H=-29.2kJ?mol-1 |
| B、P4(白磷,s)=4P(红磷,s)△H=+29.2kJ?mol-1 |
| C、P4(白磷,s)=4P(红磷,s)△H=-2244.7kJ?mol-1 |
| D、P4(白磷,s)=4P(红磷,s)△H=+2244.7kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化产物只有H2S04 |
| B、1mol As2S3发生反应,有28 mol电子转移 |
| C、该反应中As2S3既是氧化剂又是还原剂 |
| D、As2S3不可能与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性:NaOH<Mg(OH)2<Al(OH)3 |
| B、氢化物稳定性:HF>HCl>PH3 |
| C、原子半径:S>F>O |
| D、酸性:HClO>HNO3>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.045mol?L-1 |
| B、0.036mol?L-1 |
| C、0.026mol?L-1 |
| D、0.030mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①④ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com