
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)甲池中通入CH4电极的电极反应为___________________________________。
(2)乙池中A(石墨)电极的名称为________(填“正极”、“负极”或“阴极”、“阳极”), 乙池中总反应式为____________________________________ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为______mL(标准状况),丙池中______(填“C”或“D”)极析出_______g铜。
【答案】 CH4-8e-+10OH-=== CO32-+7H2O 阳极 4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3 280 D 1.6
4Ag+O2↑+4HNO3 280 D 1.6
【解析】(1)甲池为原电池,燃料在负极失电子发生氧化还原反应在碱溶液中生成碳酸盐,甲池中通入CH4极的电极反应为:CH4-8e-+10OH-=CO32-+7H2O;(2)乙池是电解池,A为阳极,B为阴极,电池中是电解硝酸银溶液生成银,硝酸和氧气,电池反应为:4AgNO3+2H2O![]() 4Ag+O2↑+4HNO3;(3)当乙池中B极质量增加5.4g为Ag,物质的量=5.4g÷108g/mol=0.05mol,依据电子守恒计算4Ag~O2~4e-,甲池中理论上消耗O2的体积=0.05mol /4×22.4L/mol=0.28L=280mL;丙为电解池C为阳极,D为阴极,电解氯化铜溶液铜离子在阴极得到电子析出铜,结合电子守恒计算2Ag~Cu~2e-,析出铜质量=0.05mol/2×64g/mol=1.6g。
4Ag+O2↑+4HNO3;(3)当乙池中B极质量增加5.4g为Ag,物质的量=5.4g÷108g/mol=0.05mol,依据电子守恒计算4Ag~O2~4e-,甲池中理论上消耗O2的体积=0.05mol /4×22.4L/mol=0.28L=280mL;丙为电解池C为阳极,D为阴极,电解氯化铜溶液铜离子在阴极得到电子析出铜,结合电子守恒计算2Ag~Cu~2e-,析出铜质量=0.05mol/2×64g/mol=1.6g。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知:①![]() ;
;
② 苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
以下是用苯作原料制备一系列化合物的转化关系图:

(1)A转化为B的化学方程式是_________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①、②物质的结构简式:
①________________,②____________________。
(3)苯的二氯代物有__________种同分异构体。
(4)有机物 的所有原子_______(填“是”或“不是”)在同一平面上。
的所有原子_______(填“是”或“不是”)在同一平面上。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色、酸性溶液中能大量共存的一组离子是( )
A.Ca2+、Na+、SO42-、MnO4-
B.K+、Fe2+、SO42-、HCO3-
C.Ba2+、K+、Mg2+、Cl-
D.Na+、Na+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(l)基态As原子的核外电子排布式为[Ar]______,有________个未成对电子。
(2) As与N是同主族元素,从原子结构角度分析:为什么As的最高价含氧酸H3AsO4是三元酸(含三个轻基),而N的最高价含氧酸HNO3是一元酸(只含一个烃基)______。
(3)比较下列氢化物的熔点和沸点,分析其变化规律及原因__________。
(4) Na3AsO3中Na、As、O电负性由大至小的顺序是______。AsO33-的空间构型为___, AsO33-中As的杂化轨道类型为_______杂化。
(5)砷化稼(GaAs)为黑灰色固体,熔点为1238℃。该晶体属于___晶体,微粒之间存在的作用力是_________。
NH3 | PH3 | AsH3 | SbH3 | |
熔点/K | 195.3 | 140.5 | 156.1 | 185 |
沸点/K | 239.6 | 185.6 | 210.5 | 254.6 |
(6)图为GaAs的晶胞,原子半径相对大小是符合事实的,则白球代表____原子。
己知GaAs的密度为5.307g·cm3, Ga和As的相对原子质量分别为69.72、74.92,求晶胞参数a=______pm (列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发展“绿色食品”是提高人类生存质量的重要措施,绿色食品指( )
A.绿颜色的营养食品
B.含叶绿素的营养食品
C.植物类营养食品
D.安全无公害的营养食品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸越稀还原产物中氮元素的化合价越低。某同学取铁铝合金与足量很稀的硝酸充分反应没有气体放出。在反应后的溶液中逐渐加入4mol·L-1NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示(不考虑沉淀的微量溶解)。下列说法不正确的是
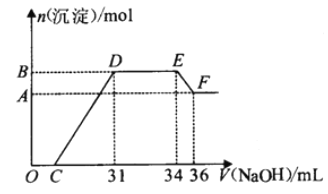
A. D点溶液中存在:c(NH4+)+c(Na+)+c(H+)=c(OH-)+c(NO3-)
B. EF段发生反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O
C. D点溶液中n(NH4+)=0.012mol
D. 由水电离产生的c(H+):O点>F点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
Ⅰ.氮氧化物的研究
(1)一定条件下,将2mol NO与2mol O2置于恒容密闭容器中发生反应:2NO(g)+O2(g) ![]() 2NO2(g),下列状态能说明该反应达到化学平衡的是(_______)
2NO2(g),下列状态能说明该反应达到化学平衡的是(_______)
A.混合气体的密度保持不变
B.NO的转化率保持不变
C.NO和O2的物质的量之比保持不变
D.O2的消耗速率和NO2的消耗速率相等
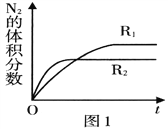
(2)已知反应. 2NO(g) ![]() N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图1所示。根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是______ (填字母序号)。
A.压强 B.温度 C.催化剂
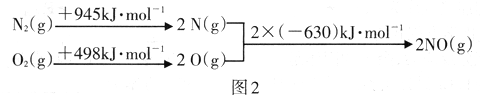
根据图2中的能量变化数据.计算反应2NO(g) ![]() N2(g)+O2(g)的ΔH=__________
N2(g)+O2(g)的ΔH=__________
Ⅱ.碳氧化物研究
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图3甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图3甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:

请回答:
①T1_____ T2(填“>”或“<”或“=”),理由是____________________。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为_________,该温度下的化学平衡常数为________ 。
②若将1mol CO和2mol H2通入原体积为1L的恒压密闭容器(图3乙)中,在T2℃下达到平衡,此时反应的平衡常数为_________;若再向容器中通入l mol CH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量_________(填“变大”或“变小”或“不变”)。
(4)一定条件下也可用NaOH溶液与CO反应生成甲酸钠,进一步反应生成甲酸来消除CO污染。常温下将a mol的CO通入2 L bmol/L NaOH 溶液中,恰好完全反应生成甲酸钠和含少量甲酸的混合溶液(假设溶液体积不变),测得溶液中c(Na+)=c(HCOO-),则该混合溶液中甲酸的电离平衡常数 Ka=____________ (用含a和b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是 ( )

A. 原子半径:W>Z>Y>X
B. 气态氢化物的稳定性:Z>W>X>Y
C. W的最高正化合价与负化合价的绝对值可能相等
D. 若X位于第VA族,则沸点:XH3<WH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com