
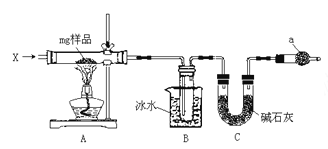
【题目】为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的 CO2 质量进行 计算,某同学设计的实验装置示意图如下:
请回答:
(1)仪器 C 的名称是__________;
(2)装置 B 中冰水的作用是__________;
(3)该同学设计的实验装置存在缺陷,有关该实验装置及实验 过程中,下列因素可能使碳酸钠的质量分数偏高的是__________。
A.样品分解不完全
B.装置 B、C 之间缺少 CO2 的干燥装置
C.产生 CO2 气体的速率太快,没有被碱石灰完全吸收
D.反应完全后停止加热,通入过量的空气
【答案】 U 型干燥管 冷凝水蒸气 AC
【解析】按照图示连接好装置后,利用气体赶净装置中的空气,X为氮气,避免空气中二氧化碳影响测定结果,固体受热分解生成的二氧化碳和水蒸气进入装置B,利用冰水混合物冷却生成的水蒸气,进入装置C中的碱石灰吸收生成的二氧化碳,最后干燥管中为碱石灰是防止空气中的二氧化碳、水蒸气进入装置C影响测定结果。则
(1)仪器C的名称是U型干燥管;(2)装置B利用冰水混合物冷却生成的水蒸气,防止水蒸气进入装置C造成误差;(3)A.样品分解不完全,测定二氧化碳质量减小,碳酸氢钠质量减小,则碳酸钠质量增大,导致碳酸钠的质量分数偏高,A正确;B.装置B、C之间缺少CO2的干燥装置,水蒸气进入装置C导致测定二氧化碳质量增大,碳酸氢钠质量增大,碳酸钠质量减小,导致碳酸钠的质量分数偏低,B错误;C.产生CO2气体的速率太快,没有被碱石灰完全吸收,测定二氧化碳质量减小,碳酸氢钠质量减小,碳酸钠质量增大导致碳酸钠的质量分数偏高,C正确;D.反应完全后停止加热,通入过量的空气,会导致空气中二氧化碳也被装置C吸收,测定碳酸氢钠质量增大,碳酸钠质量减小,导致碳酸钠的质量分数偏低,D错误;答案选AC。


科目:高中化学 来源: 题型:
【题目】请根据物质的量相关计算填空
(1)19.6 g 硫酸是_____mol H2SO4 ,1.7 gNH3 在同温同压下与_____g H2S 气体含有的氢原子数相同。
(2)在标准状况下,1.6 g 某气态氧化物 RO2 体积为 0.56L,该气体的物质的量是_____,R 的相 对原子量为_____。
(3)已知 Wg 气体 A 含有 a 个分子,那么在标准状况下,bg 气体 A 所占的体积是 _____L (其中阿 伏加德罗常数用 NA 表示)
(4)标准状况下,密度为 0.75g/L 的 NH3 与 CH4 组成的混合气体中,NH3 的体积分数_______________, 混合气体的平均摩尔质量为_____, 该气体对氢气的相对密度为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图象如下:分析图象,以下结论错误的是

A. 溶液pH≤2时,生铁发生析氢腐蚀
B. 在酸性溶液中生铁可能发生吸氧腐蚀
C. 析氢腐蚀和吸氧腐蚀的速率一样快
D. 两溶液中负极反应均为:Fe﹣2e﹣=Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三个氧化还原反应:①2FeCl3+2KI===2FeCl2+2KCl+I2②2FeCl2+Cl2===2FeCl3③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2![]() +8H2O下列有关说法正确的是
+8H2O下列有关说法正确的是
A. 还原性最强的是FeCl3
B. 氧化性的强弱顺序为:KMnO4>FeCl3 >C12
C. 若溶液中Cl-与I-共存,为了氧化I-而不氧化CI-可以向溶液中通人Cl2
D. 反应③中若生成2mol Cl2共转移5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C三种常见的短周期元素,它们的取子序数逐渐增大。A元素原子最外层电子数是次外层电子数的2倍,B元素原子最外层电子数等于其电子层数,且为C元素原子最外层电子数的一半。甲为含B的钠盐,乙为C的最高价氧化物对应的水化物,丙为含A的钠盐。 甲、乙、丙、丁四种物质之间的相互反应关系如下图:

请回答:
(1) 写出A的最高价的氧化物的电子式___________;C在周期表中的位置____________。
(2) 用有关化学用语解释丙溶液呈碱性的原因____________。
(3) 写出甲溶液与足量乙溶液反应的离子方程式: ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按单质、化合物、混合物的顺序排列的是
A. 液氧、 烧碱、 碘酒 B. 生石灰、熟石灰、 胆矾
C. 铜、 干冰、 冰水 D. 空气、 氮气、 白磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Na2SO3+2H2O+I2=Na2SO4+2HI; ②Cl2+2Fe2+=2Fe3++2Cl-;③I2+Fe2+不反应,向含SO32-、Fe2+、I-各0.1 mol的溶液中通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量的关系图正确的是
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是橙色的酸性K2Cr2O7水溶液遇乙醇迅速生成绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物
A.②④B.②③C.①③D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com