
【题目】下列各组物质按单质、化合物、混合物的顺序排列的是
A. 液氧、 烧碱、 碘酒 B. 生石灰、熟石灰、 胆矾
C. 铜、 干冰、 冰水 D. 空气、 氮气、 白磷
科目:高中化学 来源: 题型:
【题目】对比甲烷和乙烯的燃烧反应,下列叙述中正确的是( )。
①二者燃烧时现象完全相同 ②点燃前都应验纯 ③甲烷燃烧的火焰呈淡蓝色,乙烯燃烧的火焰较明亮,并有大量黑烟生成 ④二者燃烧时都有黑烟生成
A.①②B.③④C.①④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂,工业上可用NO与Cl2合成,回答下列问题:
(1)—定条件下,氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及热化学方程式和平衡常数如下表:
序号 | 热化学方程式 | 平衡常数 |
① | 2NO2(g) +NaCl(s) | K1 |
② | 4NO2(g) +2NaCl(s) | k2 |
③ | 2NO(g)+Cl2(g) | K3 |
K3=_______(用K1、K2表示)。
(2)25℃时,向体积为2L且带气压计的恒容密闭容器中通入0.08molNO和0.04molCl2发生反应:2NO(g)+Cl2(g) ![]() 2ClNO(g) △H3。
2ClNO(g) △H3。
① 下列描述能说明该反应已达到平衡状态的是_____(填序号)
a.v正(Cl2)=2v逆(NO) b.容器内混合气体的密度保持不变
c.容器内气体压强保持不变 d.容器内混合气体的平均相对分子质量保持不变
②若反应起始和平衡时温度相同,测得反应过程中压强(P)随时间(t)的变化如图I曲线a所示,则△H3______0(填“ >”、“ < ”或“不确定");若其他条件相同,仅改变某一条件时,测得其压强(P)随时间(t)的变化如图I曲线b所示,則改变的条件是_________。
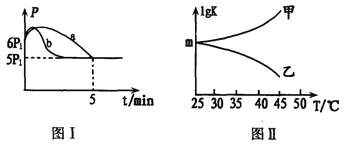
③图II是甲、乙同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是____(填“甲”或“乙”);m值为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200℃时将 16.0g NaOH 和 NaHCO3 的混合物放在密闭容器中加热到质量不再减少为止,称得剩 余固体质量为 14.8g,试回答:
(1)剩余固体的化学式是__________。
(2)原混合物中 NaOH 的质量分数__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定碳酸钠和碳酸氢钠混合样品中碳酸钠的质量分数,可通过加热分解得到的 CO2 质量进行 计算,某同学设计的实验装置示意图如下:
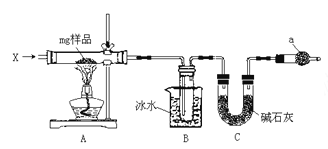
请回答:
(1)仪器 C 的名称是__________;
(2)装置 B 中冰水的作用是__________;
(3)该同学设计的实验装置存在缺陷,有关该实验装置及实验 过程中,下列因素可能使碳酸钠的质量分数偏高的是__________。
A.样品分解不完全
B.装置 B、C 之间缺少 CO2 的干燥装置
C.产生 CO2 气体的速率太快,没有被碱石灰完全吸收
D.反应完全后停止加热,通入过量的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。
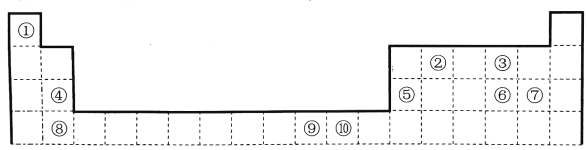
请回答下列问题:
(1)元素⑩的基态原子的价电子排布式为_________________。
(2)元素②的一种氢化物(分子中含有6个原子)是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是________。
A.分子中含有分子间的氢键
B.属于含有极性键的非极性分子
C.只含有4个sp'-s的δ键和1个P-P的π键
D.该氢化物分子中②原子采用sp2杂化
(3)下图所示为血红蛋白和肌红蛋白的活性部分(血红素)的结构式。此结构片段中含有的化学键有________(填序号)。
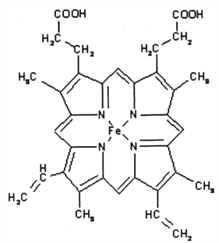
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键G. δ键 H.兀键
(4)下表为原子序数依次增大的短周期元素A~F的第一到第五电离能数据。

请回答:表中的金属元素是______(填字母);若A、B、C为原子序数依次增大的同周期相邻元素,表中显示B比A和C的第一电离能都略大,其原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】11.2g Fe加入一定量的HNO3充分反应后,生成Fe2+、Fe3+的物质的量之比为1:4,将生成的气体NXOY与一定量的O2混合后通入水中,反应后无气体剩余(NXOY+O2+H2O-HNO3 ),则通入的氧气的物质的量是
A. 0.12mol B. 0.14mol C. 0.2mol D. 0.13mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用乙醇与浓硫酸的混合液加热的方法制取乙烯。反应中常因温度而发生副反应。请选用下列装置(装置可以使用多次)完成相关实验并回答有关问题:
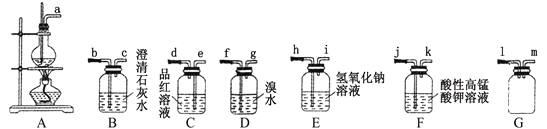
(1)制备乙烯时,常在A装置的烧瓶中加入碎瓷片,其目的是______________________;加热时要使溶液的温度迅速上升到140℃以上,因为在140℃左右易生成乙醚,该有机物的结构简式为_____________;生成乙烯的化学方程式为_____________________。
(2)乙醇与浓硫酸加热制取乙烯时,乙烯气体中常混有SO2和 CO2,为验证有副产物SO2和 CO2气体存在,上述仪器的连接顺序为a→_________________________________。
(3)某同学设计制备1,2-二溴乙烷的装置连接顺序为A→E→C→D。已知1,2-二溴乙烷的主要物理性质有:难溶于水、熔点9℃、沸点132℃、密度2.2 g·cm-3。
①E装置的作用_________________________;
②分离D装置中1,2-二溴乙烷的操作方法是加入试剂_______________ ,充分反应后进行______________操作。
③反应过程中,应将D装置放在10℃的水浴中,温度不宜过低、过高的原因是__________________________________________________。
(4)请设计验证酸性高锰酸钾溶液能将乙烯氧化为CO2的实验方案。装置连接顺序为A→_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙酸的说法中不正确的是( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有强烈刺激性气味的液体
D.乙酸分子中有四个氢原子,所以不是一元酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com