
【题目】200℃时将 16.0g NaOH 和 NaHCO3 的混合物放在密闭容器中加热到质量不再减少为止,称得剩 余固体质量为 14.8g,试回答:
(1)剩余固体的化学式是__________。
(2)原混合物中 NaOH 的质量分数__________。
【答案】 NaOH 、Na2CO3 65%
【解析】在密闭容器中进行反应,可能的反应有:NaOH+NaHCO3![]() Na2CO3+H2O、2NaHCO3
Na2CO3+H2O、2NaHCO3![]() Na2CO3+CO2↑+H2O,假设NaOH与NaHCO3恰好完全反应,则:
Na2CO3+CO2↑+H2O,假设NaOH与NaHCO3恰好完全反应,则:
NaOH+NaHCO3![]() Na2CO3+H2O △m
Na2CO3+H2O △m
40 84 18
x y 16g-14.8g=1.2g
解得:x=2.67g、y=5.6g,因x+y<16g,故16gNaOH和NaHCO3固体混合物不能恰好反应,所以存在过量问题,由于NaHCO3受热能分解,NaOH不能,因而过量物质为NaOH。
(1)由上述分析可知剩余固体物质是NaOH、Na2CO3;(2)原混合物中m(NaOH)=16g-5.6g=10.4g,因此原混合物中NaOH的质量分数为10.4g/16g×100%=65%。


科目:高中化学 来源: 题型:
【题目】把纯净的甲烷与氯气的混合气放在集气瓶中,用玻璃片盖好瓶口,放在光亮的地方一段时间后,下列说法中,不正确的是( )
A.气体发生爆炸反应
B.瓶内气体的颜色变浅
C.用一根蘸有浓氨水的玻璃棒伸入瓶内时有白烟产生
D.集气瓶壁有油状液体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(l)已知反应H2S + 2HNO3(浓)=3S↓+ 2NO2+2H2O,该反应的还原剂是_______,氧化产物是____,生成16gS转移的电子数为____。
(2)Cu2S(Cu显+1价)与一定浓度的HNO3反应生成Cu(NO3)2、CuSO4、NO和H2O,反应的化学方程式为____。
(3)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x的值为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海带中提取碘,可经过以下实验步骤完成。下列有关说法正确的是
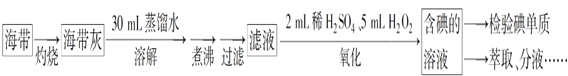
A. 灼烧过程中使用的玻璃仪器有酒精灯、坩埚、玻璃棒
B. 氧化过程中发生反应的离子方程式为 2I-+H2O2 =I2+2OH-
C. 检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明海带中含有碘单质
D. 分液时,先打开活塞放出下层液体,再关闭活塞倒出上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三个氧化还原反应:①2FeCl3+2KI===2FeCl2+2KCl+I2②2FeCl2+Cl2===2FeCl3③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2![]() +8H2O下列有关说法正确的是
+8H2O下列有关说法正确的是
A. 还原性最强的是FeCl3
B. 氧化性的强弱顺序为:KMnO4>FeCl3 >C12
C. 若溶液中Cl-与I-共存,为了氧化I-而不氧化CI-可以向溶液中通人Cl2
D. 反应③中若生成2mol Cl2共转移5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如下:
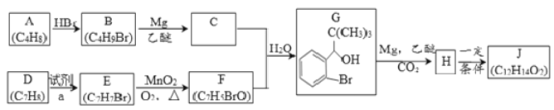
已知: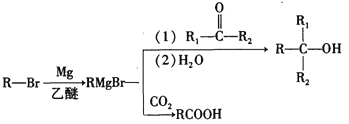
(1) D生成E的反应类型为________;
(2) F的官能团名称为________;
(3) E的含苯环同分异构体共有________ 种(含E);
(4) J是一种酯,分子中除苯环外还含有一个五元环,J的结构简式为________ ,H在一定条件下还能生成高分子化合物K,H生成K的化学方程式为________。
(5) 利用題中信总写出以乙醛和苯为原料,合成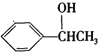 的路线流程图(其它试剂自选)。
的路线流程图(其它试剂自选)。
_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按单质、化合物、混合物的顺序排列的是
A. 液氧、 烧碱、 碘酒 B. 生石灰、熟石灰、 胆矾
C. 铜、 干冰、 冰水 D. 空气、 氮气、 白磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的结构简式可表示为![]() ,下列关于该物质的说法中正确的是( )
,下列关于该物质的说法中正确的是( )
A. 分子中最多有12个碳原子处于同一平面上 B. 该烃的一氯代物有4种
C. 分子中至少有10个碳原子处于同一平面上 D. 该烃是甲苯的同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com