
【题目】洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1) 工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为___________________
(2)漂白粉的有效成分是(填化学式)_______________________ 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式 _______________________________
(4)实验室制氯气的化学方程式为____________________________,如果想收集到纯净干燥的Cl2,应将该混合气体依次通入盛有_____和________ 的洗气瓶中。
【答案】2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO)2 CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 饱和食盐水 浓硫酸
MnCl2+Cl2↑+2H2O 饱和食盐水 浓硫酸
【解析】
(1)氯气和石灰乳反应生成氯化钙、次氯酸钙和水;
(2)漂白粉的有效成分为次氯酸钙;
(3)次氯酸钙可以和空气中的水及二氧化碳反应生成具有漂白作用的次氯酸;
(4)实验室利用浓盐酸和二氧化锰加热反应制备氯气,根据氯气中含有水蒸气和氯化氢分析判断。
(1)石灰乳和氯气反应制备漂白粉,该反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(2)漂白粉的有效成分为次氯酸钙,化学式为Ca(ClO)2;
(3)漂白粉的漂白原理是:次氯酸钙与空气中的水和CO2作用生成的次氯酸是一种很好的杀菌消毒剂,反应的化学方程式为CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO;
(4)实验室制氯气利用二氧化锰在加热的条件下氧化浓盐酸,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。浓盐酸易挥发,因此生成的氯气中含有水蒸气和氯化氢,首先利用饱和食盐水除去氯化氢,最后用浓硫酸干燥氯气,所以如果想收集到纯净干燥的Cl2应将该混合气体依次通入盛有饱和食盐水和浓硫酸的洗气瓶中。
MnCl2+Cl2↑+2H2O。浓盐酸易挥发,因此生成的氯气中含有水蒸气和氯化氢,首先利用饱和食盐水除去氯化氢,最后用浓硫酸干燥氯气,所以如果想收集到纯净干燥的Cl2应将该混合气体依次通入盛有饱和食盐水和浓硫酸的洗气瓶中。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】丙烯酸甲酯是一种重要的工业原料,某实验小组制取丙烯酸甲酯的装置如图所示:

①10.0 g丙烯酸和6.0g甲醇放置于三颈烧瓶中,连接好冷凝管,用搅拌棒搅拌,水浴加热。
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性。 ③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70-90℃馏分。
可能用到的信息:
沸点 | 溶解性 | 着火点(闪点) | 毒性 | |
丙烯酸 | 1420C | 与水互溶,易溶于有机溶剂 | 540C | 有毒 |
甲醇 | 650C | 与水互溶,易溶于有机溶剂 | 110C | 有毒 |
丙烯酸甲酯 | 80.50C | 难溶于水,易溶于有机溶剂 | 不详 | 无毒 |
(注闪点低于500C属于极易燃烧物质)回答下列问题:

(1)仪器c的名称是____________。
(2)混合液用5% Na2CO3溶液洗涤的目的是_____________.
(3)请写出配制100 g 5% Na2CO3溶液所使用的玻璃仪器____________。
(4)关于产品的蒸馏操作(夹持装置未画出),下图中有2处错误,请分别写出_____________、________________________.
为检验产率,设计如下实验:
①.油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5 mol/L的KOH溶液10.00 mL,加热使之完全水解。
②.用酚酞做指示剂,向冷却后的溶液中滴加0.5 mol/L的HCI溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00 mL。
(5)计算本次酯化反应丙烯酸的转化率____。
(6)请列举2条本实验中需要采取的安全防护措施___________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是
A. ρ=![]() B. w=
B. w=![]()
C. w=![]() D. c=
D. c=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合溶液中,可能大量含有的离子如下表:
阳离子 | H+、K+、Al3+、NH |
阴离子 | OH-、SO42—、CO32—、AlO2— |
将Na2O2逐渐加入上述混合溶液中并微热,产生沉淀和气体如图所示。

下列说法不正确的是:
A. 上述混合溶液中一定大量含有H+、NH4+、Al3+、Mg2+、SO42—
B. 图中a=4
C. b=7;c=9
D. 此溶液还需要用焰色反应继续检验,才能确定溶液准确组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2既是温室气体,也是重要的化工原料,二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g) ![]() N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/(mol/L)/\时间/min | 0 | 10 | 20 | 30 | 40 |
NO | 2.0 | 1.16 | 0.40 | 0.40 | 0.6 |
N2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
①若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:3:3,则达到新平衡时NO的转化率____(填“升高”或“降低”),△H____0(填“>”或“<”)。
②根据图表数据分析T1℃时,该反应在0~10min内的平均反应速率v(N2)=__mol·L-1·min-1;计算该反应的平衡常数K=___。
③若30min后只改变某一条件,据上表中的数据判断改变的条件可能是____________(填字母编号)。
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
(2)工业上用CO2和H2反应合成二甲醚(CH3OCH3)。二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:______________。
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。若某次捕捉后得到pH=10 的溶液,则溶液c(CO32-)∶c(HCO3-)=____________。[常温下K1(H2CO3)=4.4×10-7、 K2(H2CO3)=5×10-11]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O。
实验探究一:学生甲利用如图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成。回答下列问题:

(1)仪器组装完成后,夹好止水夹,__________________________________,则说明装置A的气密性良好。
(2)下列实验步骤中,正确的操作顺序是____________(填序号)。
①打开止水夹;②熄灭C处的酒精喷灯;③C处冷却至室温后,关闭止水夹;④点燃C处的酒精喷灯;⑤收集氢气并验纯
实验探究二:
(3)学生乙取少量样品于烧杯中,加入过量稀硫酸,并作出如下假设和判断,结论正确的是 ______。
A.若固体全部溶解,说明样品中一定含有Fe2O3,一定不含有Cu2O
B.若固体部分溶解,说明样品中一定含有Cu2O,一定不含有Fe2O3
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,说明样品一定含有Fe2O3和Cu2O
D.若固体全部溶解,再滴加KSCN溶液,溶液变红色,说明样品一定含有Fe2O3
另取少量样品于试管中,加入适量的浓硝酸,产生红棕色气体,证明样品中一定含有________,写出产生上述气体的化学方程式:____________________。
实验探究三:
(4)学生丙取一定量样品于烧杯中,加入足量的稀硫酸,反应后经过滤得到固体6.400g,测得滤液中Fe2+有2.000mol,则样品中n(Cu2O)=________________________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】价电子式为4s24p1的元素,在周期表中的位置是( )
A. 第四周期第ⅠA族B. 第四周期第ⅢA族
C. 第五周期第ⅠA族D. 第五周期第ⅢA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的量热计中,将100mL0.50mol/L CH3COOH溶液与100mL0.55mol/LNaOH溶液混合,温度从25.0℃升高到27.7℃。已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J·℃-1,生成溶液的比热容为4.184J·g-1·℃-1,两溶液的密度均近似为lg/mL.下列说法错误的是
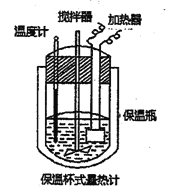
A. 若量热计的保温瓶绝热效果不好,则所测△H偏大
B. 该实验测得反应放出的热量为2665.7J
C. 该实验测得的中和热ΔH为-45.2kJ/mol
D. 所加NaOH溶液过量,目的是保证CH3COOH溶液完全被中和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com