
【题目】工业上可利用CO2和H2生成甲醇,热化学方程式如下: CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=Q1kJmol﹣1
又查资料得知:①CH3OH(l)+ ![]() O2(g)CO2(g)+H2(g)△H=Q2kJmol﹣1
O2(g)CO2(g)+H2(g)△H=Q2kJmol﹣1
②H2O(g)=H2O(I)△H=Q3kJmol﹣1
则表示甲醇的燃烧热的热化学方程式为 .
【答案】CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3)kJ?mol﹣1
O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3)kJ?mol﹣1
【解析】解:①CO2(g)+3H2(g)CH3OH(l)+H2O (g)△H=Q1kJmol﹣1②CH3OH(l)+ ![]() O2(g)CO2(g)+2H2(g)△H=Q2kJmol﹣1③H2O(g)=H2O(l)△H=Q3kJmol﹣1 , 依据盖斯定律①×2+②×3+③×2得到: 表示甲醇的燃烧热的热化学方程式为:CH3OH(l)+
O2(g)CO2(g)+2H2(g)△H=Q2kJmol﹣1③H2O(g)=H2O(l)△H=Q3kJmol﹣1 , 依据盖斯定律①×2+②×3+③×2得到: 表示甲醇的燃烧热的热化学方程式为:CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJmol﹣1 ,
O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJmol﹣1 ,
所以答案是:CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJmol﹣1 .
O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJmol﹣1 .


科目:高中化学 来源: 题型:
【题目】已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。设X的原子序数为a,则下列说法不正确的是( )

A. Y的原子序数可能为a-17 B. Z的原子序数可能为a+31
C. X、Y、Z可能为短周期元素 D. Y与Z的原子序数之和可能为2a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y 各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表,下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10﹣3 mol/(Lmin)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的溶液,造成浓度偏高的操作是
A.定容时,滴加蒸馏水超过刻度线
B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中
D.定容时,眼睛仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3Cl2+6KOH=5KCl+KClO3+3H2O中,氧化产物与还原产物的物质的量之比为( )
A. 1:3 B. 1:2 C. 1:5 D. 5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为倡导“低碳”,减小CO2对环境的影响,需对CO2进行创新利用研究.T1℃使,将将9mol CO2和12mol H2充入3L密闭容器中,发生反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p0 . 改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示.下列说法错误的是( ) 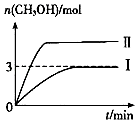
A.曲线Ⅱ对应的条件改变是增大压强
B.T2℃时,上述反应平衡常数为0.52,则T2>T1
C.在T1℃,若起始时向容器充入4.5 mol CO2、6 mol H2 , 平衡时容器内压强P1> ![]()
D.在T1℃,若起始时向容器中充入4.5 mol CO2、5 mol H2、5 mol CH3OH(g)和5 mol H2O(g),则达平衡前v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.配制一定物质的量浓度的溶液,向容量瓶加水至液面离刻度线1~2 cm时,改用胶头滴管定容
B.向某溶液中先加入Ba(NO3)2溶液,再加入足量的HNO3溶液,产生白色沉淀,则该溶液中一定含有SO ![]()
C.分液操作时,将下层液体先放出,然后关闭旋塞,将上层液体从上口倒出
D.将油脂与氢氧化钠溶液混合充分反应后,再加入热的饱和食盐水,则可析出肥皂的主要成分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com