
����Ŀ������粒㷺Ӧ���빤ũ�����У�����������ͼ���£��ش��������⣺
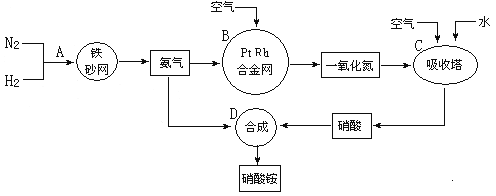
��1����������ҵ������������У�B�豸�������� ���ڷ�Ӧ�е����������� ��
��2�������������У�N2��H2�ϳ�NH3���õĴ����� ���ںϳɰ����豸(�ϳ���)�У������Ƚ�������Ŀ���� ���ںϳ��������������ͨ�������Ŀ���� ��
��3����ѧ����(NH3)Ϊȼ�Ͽ������͵�ȼ�ϵ������������ɴ���O2�����ӵ� MnO3�������ʣ�����ܷ�ӦΪ��4NH3+3O2=2N2+6H2O�������ĵ缫��ӦʽΪ ��
��4��ij���ʳ���NH3�Ʊ�NH4NO3����֪����NH3��NO�IJ�����96%��NO��HNO3�IJ�����92%������HNO3����ȥ��NH3������Լռ�ܺ�NH3����(�������������)�� %��(ȡ��λ��Ч����)
��5���������һ�ֳ��õĵ��ʣ���ʹ�øû���ʱ��������Է���һ��ʹ�ã������� ��
���𰸡�
��1������¯��NO��
��2������ý���������ȣ���Լ��Դ�� ��ʹNOȫ��ת����HNO3
��3��2NH3+3O2�� - 6e��= N2+ 3H2O
��4��53% ��
��5��NH4+ˮ������ԣ�����ϴٽ���ˮ����
��������
�����������1��B�а���������������һ����������װ������Ϊ����¯(��������)����Ӧ�Ļ�ѧ����ʽΪ��4NH3+5O2![]() 4NO+6H2O����Ӧ������������NO���ʴ�Ϊ������¯(��������)��NO��
4NO+6H2O����Ӧ������������NO���ʴ�Ϊ������¯(��������)��NO��
��2��N2��H2�ϳ�NH3���õĴ���Ϊ����ý���ϳɰ��ķ�Ӧ���ڷ��ȷ�Ӧ����Ӧ�����л�ų��������ȣ����Ƚ��������Գ���������ȣ���Լ��Դ�����������ж���������ˮ��Ӧ���������NO��ͨ�������NO�ܱ������е���������Ϊ����������������������ˮ��Ӧ�������ᣬ����ʹNOѭ�����ã�ȫ��ת��Ϊ����ʴ�Ϊ������ý���������ȣ���Լ��Դ����ʹNOѭ�����ã�ȫ��ת����HNO3��
��3����������ɴ���O2�����ӵ� MnO3�������ʣ�����ܷ�ӦΪ��4NH3+3O2=2N2+6H2O����������������Ӧ���缫��ӦʽΪ2NH3+3O2�� - 6e��= N2+ 3H2O���ʴ�Ϊ��2NH3+3O2�� - 6e��= N2+ 3H2O��
��4�����ݵ�ԭ���غ��֪��NH3��NO��HNO3����1mol�����ɵõ���������ʵ���Ϊ��1mol��96%��92%=0.8832mol������HNO3+NH3�TNH4NO3��֪��Ӧ���ĵİ��������ʵ���Ϊ��0.8832mol������������֮�ȵ������ʵ���֮��������HNO3����ȥ��NH3������ռ�ܺ�NH3�����İٷ���Ϊ��![]() ��100%��53%���ʴ�Ϊ��53%��
��100%��53%���ʴ�Ϊ��53%��
��5��������е�NH4+ˮ������ԣ�����ϴٽ���ˮ�⣻ʹ��ʱӦ��������Է���һ��ʹ�ã��ʴ�Ϊ��NH4+ˮ������ԣ�����ϴٽ���ˮ�⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʵ����ͬһԭ�����͵���( )
A��SO2��FeSO4��Һʹ���Ը�����ص���ɫ��ȥ
B��Ũ�����Ũ���᳤�ڱ�¶�ڿ�����Ũ�Ƚ���
C��������pH��ֽ�ⶨŨ�����������ˮ��pH
D������������Һ���Ȼ�����Һ�ڿ��������ɲ��ܵõ���Ӧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ�жϣ�����˵����ȷ����(����)

A. װ�â��װ�â��и�����Ӧ����Fe-2e-Fe2+
B. װ�â��װ�â���������Ӧ����O2+2H2O+4e-4OH-
C. װ�â��װ�â��������е������Ӿ����Ҳ��ձ��ƶ�
D. �ŵ�����У�װ�â�����ձ���װ�â��Ҳ��ձ�����Һ��pH������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ������������ȷ��һ����
A�����ӻ�������һ���������Ӽ�
B�����ʷ����о������ڻ�ѧ��
C��ȫ���ɷǽ���Ԫ���γɵĻ������в����ܺ������Ӽ�
D�����й��ۼ��Ļ�����һ���ǹ��ۻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʲ�������ʳƷ���Ӽ����ǣ� ��
A. �Ȱ��ᵥ�� B. ������ C. ɽ����� D. �����谷
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A�����������������ԭ�ӱ���ԭ��ȡ���������ֲ�ͬ�ṹ����
B����ȩ��ʹ�����ʱ��ԣ�������ʳƷ������
C���״�������ˮ����֮����������ʹ�״���ˮ����������ǿ
D���ױ��뱽��Ϊͬϵ�����ʹKMnO4������Һ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����ᡢ�����������������������˵����ȷ����
A�������������������ƶ��dz�����θ���кͼ�
B�����������Ƕп����������������������������
C��ˮ�ࡢ��觡�����ɸ���ǹ����ι�ҵ��Ʒ
D��������ˮʱ��������ɱ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������NaBH4/H2O2ȼ�ϵ�أ�DBFC���Ľṹ��ͼ��ʾ������֪���⻯������Ϊ-1�ۣ����йظõ�ص�˵����ȷ����
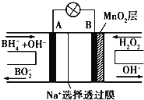
A���缫B�����к�MnO2�㣬MnO2����ǿ������
B����ظ������ĵ缫��Ӧ��BH4-+8OH--8e-��BO2-+6H2O
C���ŵ�����У�Na+������������Ǩ��
D���ڵ�ط�Ӧ�У�ÿ����1L6mol/LH2O2��Һ��������������·�еĵ���Ϊ6NA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaClO3��NaI�����ʵ���֮��1��1�������ƿ�У������������ᣬ��ˮԡ���ȣ���Ӧ����NaClO3��NaIǡ����ȫ��Ӧ������I2��Na2SO4��H2O���������ػ�ɫ������X����XΪ
A��Cl2 B��Cl2O C��ClO2 D��Cl2O3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com