
| A.熔点:MgBr2<SiCl4<BN |
| B.冰和干冰均为分子晶体,冰的沸点、密度都高于干冰 |
| C.第ⅤA族元素的几种气态氢化物中,NH3是稳定性最高的氢化物 |
| D.同周期ⅦA族元素的氧化物对应水化物的酸性一定强于ⅥA族 |
科目:高中化学 来源:不详 题型:填空题
| 元素 | 有关信息 |
| X | 最外层电子数是次外层的2倍 |
| Y | 元素的主要化合价为-2价 |
| Z | 其单质及化合物的焰色为黄色 |
| M | 与X同主族,其单质为半导体材料 |
| N | 其单质在Y单质中燃烧,发出明亮的蓝紫色火焰 |
 2NY3(g)。温度分别为T1和T2时,NY3的体积分数随时间变化如下图。该反应的△H 0(填“>”、“<”或“=”,下同);若T1、T2时该反应的化学平衡常数分别为K1、K2,则K1 K2。
2NY3(g)。温度分别为T1和T2时,NY3的体积分数随时间变化如下图。该反应的△H 0(填“>”、“<”或“=”,下同);若T1、T2时该反应的化学平衡常数分别为K1、K2,则K1 K2。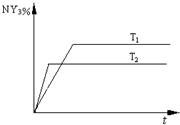
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.R氢化物的沸点高于Y氢化物的沸点 |
| B.R元素基态原子与W元素基态原子未成对电子数相同 |
| C.W与Y形成的化合物能与强碱溶液反应,但不能与任何酸反应 |
| D.R与Y形成的化合物和W与Y形成的化合物的晶体类型相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| a | | | |||||||||||||||
| b | | | | c | d | e | f | | |||||||||
| g | h | i | j | | k | l | m | ||||||||||
| n | | | | | | | o | | | | | | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③④ | B.②④ | C.①②④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已经制得了 IBr、ICl 等卤素互化物 |
| B.已经制得 I2O5 等碘的氧化物 |
| C.已经制得了I (NO3)3、I (ClO4)3·2H2O等含 I3+ 离子化合物 |
| D.碘(I2)易溶于KI等碘化物溶液,形成I3- 离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com