
【题目】乙醇做为可再生能源比化石能源具有较大的优势,如图为乙醇燃料电池,该电池的总反应方程式为C2H5OH+3O2=2CO2+3H2O。下列关于该电池叙述错误的是
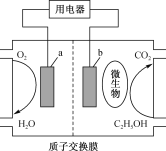
A.a极与用电器的正极相接B.该装置将化学能转化为电能
C.质子(H+)由装置左侧向右侧移动D.该装置的电解质溶液呈酸性
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.破坏乙烯分子里![]() 所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
B.乙烯分子和苯分子都能使溴水褪色,两者褪色原理相同
C.因为甲烷和苯都不能被酸性 KMnO4 溶液氧化,所以两者都不能发生氧化反应
D.甲烷和苯都能和氯气发生取代反应,但是两者发生反应时需要的条件不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。
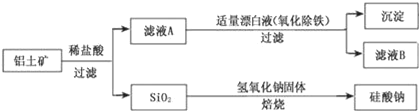
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①该过程中涉及某氧化还原反应如下,请完成:__Fe2+___ClO-+( )___=____Fe(OH)3↓+__C1﹣+( )。
②检验滤液B中是否还含有铁元素的方法为:________(注明试剂、现象)。
③将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___(填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
④由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、____(填操作名称)、洗涤。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___(填代号)。
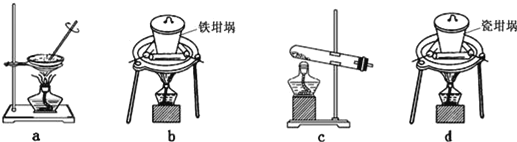
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlH3是一种储氢材料,可作为固体火箭推进剂。通过激光加热引发AlH3的燃烧反应,燃烧时温度随时间变化关系如下图所示。燃烧不同阶段发生的主要变化如下:
2AlH3(g)=2Al(s)+3H2(g) △H1 H2(g)+![]() O2(g)=H2O(g) △H2 Al(s)= Al(g) △H3 Al(g) +
O2(g)=H2O(g) △H2 Al(s)= Al(g) △H3 Al(g) +![]() O2(g)=
O2(g)=![]() Al2O3(s) △H4
Al2O3(s) △H4
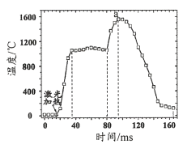
下列分析正确的是
A.AlH3燃烧需要激光加热引发,所以AlH3燃烧是吸热反应
B.其他条件相同时,等物质的量的Al(s)燃烧放热大于Al(g)燃烧放热
C.在反应过程中,a点时物质所具有的总能量最大
D.2AlH3(s)+3O2(g)=Al2O3(s)+3H2O(g) △H=△H1+3△H2+2△H3+2△H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率
4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率![]() x
x
A. ![]() (O2) = 0.01mol·(L·s) –1 B.
(O2) = 0.01mol·(L·s) –1 B. ![]() (NO) = 0.008mol·(L·s) –1
(NO) = 0.008mol·(L·s) –1
C. ![]() (H2O) = 0.006mol·(L·s) –1 D.
(H2O) = 0.006mol·(L·s) –1 D. ![]() (NH3) = 0.002mol·(L·s) –1
(NH3) = 0.002mol·(L·s) –1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I磷酸氯喹是治疗新型肺炎的潜力药。磷酸是合成该药的初级原料之一,沸点高,难挥发。化学兴趣小组设计了合成磷酸的流程如图。
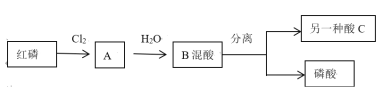
回答下列问题
(1)将一定了的红磷与氯气置于容积为2L的恒温恒容(温度,体积均不变)反应器中制取A,各物质的物质的量与时间关系如图
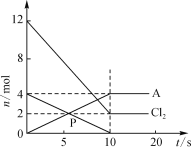
①前10s消耗的氯气为________mol,该反应的化学方程式为_________(A用化学式表示)
②前10s的平均反应速率v(Cl2)=________
(2)将A加入热水中,生成两种酸。一种为磷酸,反应过程各元素化合价不变。
①另一种是酸C是________(写名称)
②A与热水反应的化学方程式为________
II(1)将反应Cu+2FeCl3=2FeCl2+CuCl2设计成原电池,完成该原电池的装置示意图,并作相应标注(标明正负极材料及电解质溶液的名称,电子移动方向、离子移动方向)________

(2)该装置中负极的电极方程式为________。
(3)若在反应过程中电极减轻3.2g,则在导线中通过电子_____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物L具有特殊的光学性质,可用于光电材料,其合成路线如下:
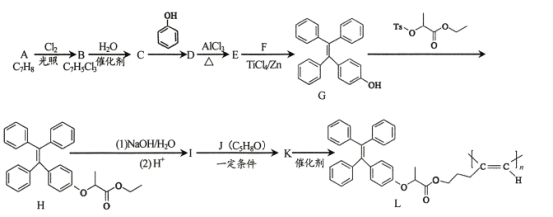
已知:
i.有机物可用键线式表示,如![]() 可表示为
可表示为
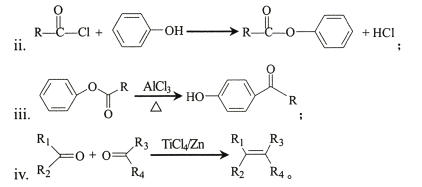
(1) A—B的化学方程式为____。
(2)D的结构简式为____。
(3)E中含有的含氧官能团为____ 。
(4) G—H的反应类型为____。
(5)I—K的化学方程式为____。
(6)下列说法正确的是______填字母序号)。
a.A分子中所有碳原子均在同一平面 b.C的结构简式为![]()
c.F+F—G的副产物中有2种互为顺反异构体 d.1 mol H最多能与2 molNaOH反应
(7)乳酸乙酯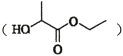 是合成
是合成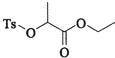 的中间体。下图是某同学设计的合成乳酸乙酯的流程。
的中间体。下图是某同学设计的合成乳酸乙酯的流程。
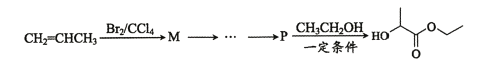
请写出M-P的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).下列说法错误的是( )

A. A、B、D可能是钠及其化合物 B. A、B、D可能是镁及其化合物
C. A、B、D可能是铝及其化合物 D. A、B、D可能是非金属及其化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氯乙烯是制作装修材料的最常用原料,失火时聚氯乙烯在不同的温度下,发生一系列复杂的化学变化,产生大量有害气体,其过程大体如下:

下列说法不正确的是
A. 聚氯乙烯的单体可由乙烯与HCl加成而得
B. 上述反应中①属于消去反应,④属于(脱氢)氧化反应
C. 火灾中由聚氯乙烯产生的有害气体中含HCl、CO、C6H6等
D. 在火灾现场,可以用湿毛巾捂住口鼻,并弯下腰尽快远离现场
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com