
【题目】下列叙述错误的是( )
A.氦气可用于填充飞艇
B.氯化铁可用于硬水的软化
C.石英砂可用于生产单晶硅
D.聚四氟乙烯可用于厨具表面涂层
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】将适量的MO2粉末投入热水中,一边搅拌,一边通入SO2气体,结果得到白色不溶物X,已知X既是氧化产物又是还原产物.下列判断错误的是( )
①MO2具有氧化性②白色不溶物X为MSO2③白色不溶物X为MSO4④白色不溶物X为MS.
A.①②
B.③④
C.②④
D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其化合物的说法正确的是( )
A.Mg和Al都可以用电解法冶炼得到
B.Mg和Fe在一定条件下与水反应都生成H2 和对应的碱
C.Fe和Cu常温下放入浓硝酸中发生的现象相同
D.Na2O和Na2O2与CO2反应产物也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g) + 3Y(g) ![]() 2Z(g),有关下列图像的说法不正确的是
2Z(g),有关下列图像的说法不正确的是
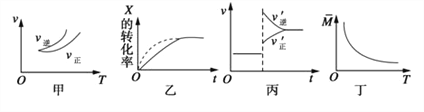
A. 依据图甲可判断正反应为放热反应
B. 在图乙中,虚线可表示使用了催化剂
C. 若正反应的ΔH<0,图丙可表示升高温度使平衡向逆反应方向移动
D. 由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应涉及H2O、ClO-、NH![]() 、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是( )
、H+、N2、Cl-六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是( )

A.该反应的还原剂是Cl-
B.消耗1 mol还原剂,转移6 mol电子
C.氧化剂与还原剂的物质的量之比为2∶3
D.反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的氧化剂是________,还原剂是________,每生成1 mol Na2FeO4转移________mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用。________________________________
________________________________________________________________________。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO![]() 、Cl-、H2O。
、Cl-、H2O。
①写出并配平湿法制高铁酸钾反应的离子方程式:___________________________。
②每生成1 mol FeO![]() 转移________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________mol。
转移________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题?___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是当今材料科学研究的前沿,指研究、开发出的直径从几纳米至几十纳米的材料,1纳米(nm)=10—9m,如果将“纳米材料”分散到液体分散剂中,下列说法一定正确的是
A.有丁达尔效应 B.不能吸附溶液中悬浮物
C.不能透过滤纸 D.所得分散系不稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.由中科院等离子体物理研究所自主研制的全超导托卡马克实验装置(俗称“人造太阳”)正在接受技术升级。它是目前世界上唯一能达到持续400秒、中心温度大于2 000万摄氏度实验环境的全超导托卡马克核聚变实验装置。人造太阳是利用氘、氚核聚变反应释放巨大能量原理而实现的,氚可在反应堆中通过锂再生。下列说法不正确的是________。
a.氕、氘、氚三种元素在周期表中的位置不同
b.20 g D2O含有的中子数为6.02×1024个
c.在隔绝空气和高温下LiCl与金属钠反应可获得金属锂
Ⅱ.部分元素在周期表中的位置如下:

请回答下列问题:
(1)元素C在周期表中的位置为________。
(2)B元素最高价氧化物对应的水化物的碱性比KOH的碱性________(填“强”或“弱”)。
(3)写出工业上制备D的化学方程式:________________________,请指出D单质的另一种主要用途________________________。
(4)用化学方程式证明E、F元素非金属性强弱:_________________________。
(5)用电子式表示F的氢化物的形成过程:_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com