
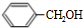 ,则G为
,则G为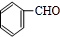 ,H为
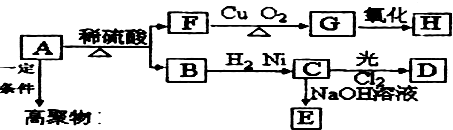
,H为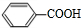 .A在酸性条件下水解生成F与B,结合A的分子式可知,A含有1个酯基,故B的分子式为C4H6O2,含有1个羧基,A的不饱和度为
.A在酸性条件下水解生成F与B,结合A的分子式可知,A含有1个酯基,故B的分子式为C4H6O2,含有1个羧基,A的不饱和度为| 2×11+2-12 |
| 2 |
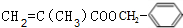 ,A发生加聚反应生成高聚物为
,A发生加聚反应生成高聚物为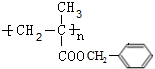 ,C与氢氧化钠反应生成E为(CH3)2CHCOONa,C与氯气发生取代反应生成D为(CH3)2CH(Cl)COOH或ClCH2CH(CH3)COOH,据此解答.
,C与氢氧化钠反应生成E为(CH3)2CHCOONa,C与氯气发生取代反应生成D为(CH3)2CH(Cl)COOH或ClCH2CH(CH3)COOH,据此解答.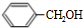 ,则G为
,则G为 ,H为
,H为 .A在酸性条件下水解生成F与B,结合A的分子式可知,A含有1个酯基,故B的分子式为C4H6O2,含有1个羧基,A的不饱和度为
.A在酸性条件下水解生成F与B,结合A的分子式可知,A含有1个酯基,故B的分子式为C4H6O2,含有1个羧基,A的不饱和度为| 2×11+2-12 |
| 2 |
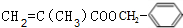 ,A发生加聚反应生成高聚物为
,A发生加聚反应生成高聚物为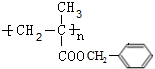 ,C与氢氧化钠反应生成E为(CH3)2CHCOONa,C与氯气发生取代反应生成D为(CH3)2CH(Cl)COOH或ClCH2CH(CH3)COOH,
,C与氢氧化钠反应生成E为(CH3)2CHCOONa,C与氯气发生取代反应生成D为(CH3)2CH(Cl)COOH或ClCH2CH(CH3)COOH,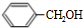 ,分子中含有的官能团结构简式是:-OH,故答案为:-OH,故答案为:-OH;
,分子中含有的官能团结构简式是:-OH,故答案为:-OH,故答案为:-OH;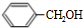 ),可以有一个侧链为-OCH3,可以有2个侧链为-OH、-CH3,有邻、间、对三种位置,符合条件的同分异构体共有4种,故答案为:4;
),可以有一个侧链为-OCH3,可以有2个侧链为-OH、-CH3,有邻、间、对三种位置,符合条件的同分异构体共有4种,故答案为:4;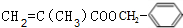 +H2O
+H2O| 稀硫酸 |
| △ |
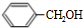 +CH2=C(CH3)COOH;
+CH2=C(CH3)COOH;| 催化剂 |
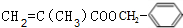
| 催化剂 |
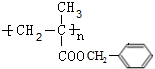 ,
,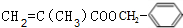 +H2O
+H2O| 稀硫酸 |
| △ |
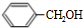 +CH2=C(CH3)COOH;
+CH2=C(CH3)COOH;| 催化剂 |
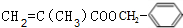
| 催化剂 |
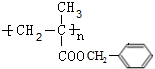 .
.


 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:
| A、A的转化率变小 |
| B、平衡向逆反应方向移动 |
| C、D的质量百分数变大 |
| D、a<c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.8g | B、5.6g |
| C、11.2g | D、1.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
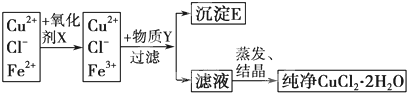
查看答案和解析>>
科目:高中化学 来源: 题型:
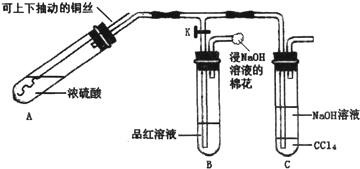
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com