
 2NH3 在恒容密闭容器中进行,达到平衡状态的标志是
2NH3 在恒容密闭容器中进行,达到平衡状态的标志是 | 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| C(NH3)/mol·L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
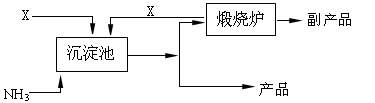
 2NH3(g);△H=-93 KJ·mol-1(2分)
2NH3(g);△H=-93 KJ·mol-1(2分) 2NH3(g);△H=-93 KJ·mol-1。
2NH3(g);△H=-93 KJ·mol-1。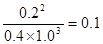 。若往平衡体系中加入H2、N2和NH3各2mol,则此时H2、N2和NH3的浓度分别为2.0mol/L、1.4mol/L、1.2mol/L,所以
。若往平衡体系中加入H2、N2和NH3各2mol,则此时H2、N2和NH3的浓度分别为2.0mol/L、1.4mol/L、1.2mol/L,所以 >0.1,所以平衡向逆反应方向移动。
>0.1,所以平衡向逆反应方向移动。

科目:高中化学 来源:不详 题型:单选题
| A.一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 |
| B.氢氧燃料电池的能量转换形式仅为化学能转化为电能 |
| C.在NH4HSO4溶液中由于NH4+的水解促进了水的电离,所以水的电离程度增大 |
D.在一密闭容器中发生2SO2+O2 2SO3反应,增大压强,平衡会正向移动, 2SO3反应,增大压强,平衡会正向移动,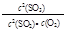 的值增大 的值增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
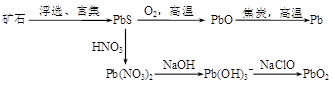
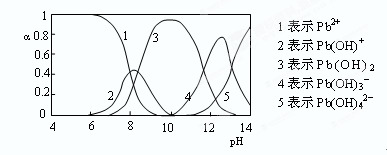
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.△H>0的反应,常温下一定不能自发进行 |
B.用0.1mol/LNaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线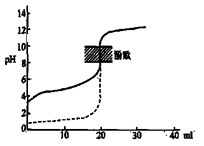 |
| C.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 |
D.恒容密闭容器中进行的反应3A(g) 2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变 2B(g)+C(s),在其它条件不变的情况下,再充入一定量的A气体,A的转化率不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
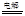 2OH?+H2↑+Cl2↑
2OH?+H2↑+Cl2↑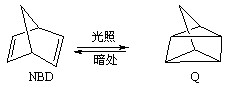 ,利用该反应可以贮存太阳能,则NBD的内能比Q的内能高
,利用该反应可以贮存太阳能,则NBD的内能比Q的内能高| 化学键 | N≡N | H?O | N?H | O=O |
| 键能/kJ·mol-1 | 945 | 463 | 391 | 498 |
 2NH3(g)+ 3/2O2(g);△H=+630kJ·mol-1
2NH3(g)+ 3/2O2(g);△H=+630kJ·mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H3BO3的酸性与H2CO3的酸性 |
| B.向Ag2CrO4浑浊液中加NaCl溶液,有AgCl沉淀生成,Ksp (Ag2CrO4) 与Ksp(AgCl) |
| C.I2在KI溶液中和在水中的溶解度 |
| D.相同温度下,lO ml O.l mol·l一的醋酸与100 ml O.01 mol·L一的醋酸中的H+物质的量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 (g)+
(g)+ 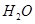 (g)=
(g)=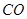 (g)+
(g)+ (g)
(g) 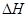 = +
= +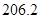
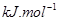
 (g)+
(g)+ 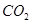 (g)=
(g)=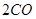 (g)+
(g)+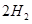 (g)
(g)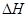 = +
= +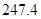
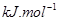
 (g)与
(g)与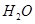 (g)反应生成
(g)反应生成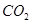 (g)和
(g)和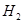 (g)的热化学方程式为 。
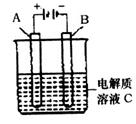
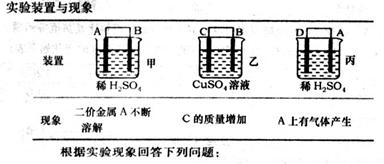
(g)的热化学方程式为 。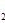 O的热分解也可得到H
O的热分解也可得到H ,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是 、 。
,高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A、B表示的物质依次是 、 。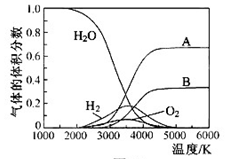
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.纯锌与稀硫酸反应时,为加快速率可滴入少量硫酸铜溶液 |
| B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C.一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D.对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com