
 4��(NH4)2SO4��ҪС����ˮ�⣻���л�ԭ�ԣ��������������ȶ��������ǽ��̷�(FeSO4?7H2O)���������������ʵ�����Ͽ��Ƶ�Ħ���ξ��������ͼ��
4��(NH4)2SO4��ҪС����ˮ�⣻���л�ԭ�ԣ��������������ȶ��������ǽ��̷�(FeSO4?7H2O)���������������ʵ�����Ͽ��Ƶ�Ħ���ξ��������ͼ�� (NH4)2SO4?FeSO4?6H2O����������ͼ�ش�
(NH4)2SO4?FeSO4?6H2O����������ͼ�ش�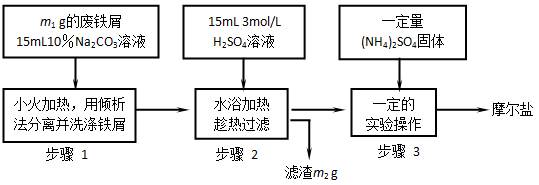

 ����־�Ĥʱ��ֹͣ���ȡ�Ϊʲô�������ɣ� ���辭����ʵ����������� ��������������ѹ���ˣ�����ˣ��ȵõ���Ϊ����
����־�Ĥʱ��ֹͣ���ȡ�Ϊʲô�������ɣ� ���辭����ʵ����������� ��������������ѹ���ˣ�����ˣ��ȵõ���Ϊ����| A����̪ | B������ | C��ʯ�� | D������Ҫ |
 3Fe2+
3Fe2+  �У���������ȷֽ��������
�У���������ȷֽ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
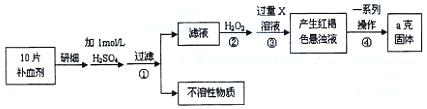
 ��ش��������⣺
��ش��������⣺ ��Ԫ�غ����IJⶨ����5Fe2++MnO4��+8H+��5Fe3++Mn2++4H2O��
��Ԫ�غ����IJⶨ����5Fe2++MnO4��+8H+��5Fe3++Mn2++4H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 �أ���ԭ��������������W��Y���������ǵ����������Ҫ���ʣ�X�Ļ�̬ԭ�Ӻ�����7��ԭ�ӹ������˵��ӣ�Z���γɺ�ɫ����ש��ɫ����
�أ���ԭ��������������W��Y���������ǵ����������Ҫ���ʣ�X�Ļ�̬ԭ�Ӻ�����7��ԭ�ӹ������˵��ӣ�Z���γɺ�ɫ����ש��ɫ����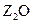 �ͺ�ɫ��ZO���������
�ͺ�ɫ��ZO���������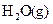 __________���ǿ������������
__________���ǿ������������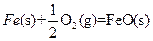
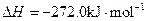

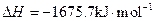
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 ������������FeO42-����
������������FeO42-����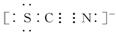
 3+����ΪFeO42-����д�������ӷ�Ӧ����ʽ__________��
3+����ΪFeO42-����д�������ӷ�Ӧ����ʽ__________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
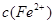 �ı仯��ͼ��ʾ���������ӷ���ʽ�������( )
�ı仯��ͼ��ʾ���������ӷ���ʽ�������( )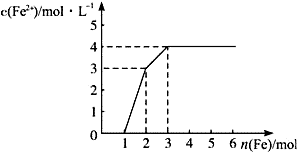
| A��0��1 : Fe+ NO3��+4H+=Fe3++ NO��+2H2O | B��1��2 : Fe+2Fe3+ =3Fe2+ |
| C��2��3 : Fe+Cu2+��Fe2++Cu | D��0��3 : 3Fe+2Fe3++2Cu2+ =5Fe2++2Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.15mol/L | B��0.3mol/L | C��0.225mol/L | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���п�ȼ��������� | B��û�г������� |
| C���к��ɫ�������� | D���а�ɫ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3)3��NO��H2O���ܽ�1mol Fe3O4����ԭ��������
3)3��NO��H2O���ܽ�1mol Fe3O4����ԭ��������| A��1/2mol | B��1/3mol | C��3mol | D��9mol |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com