
【题目】下列溶液中,C1-的物质的量浓度最大的是
A.300 mL0.1 mol/L NaCl溶液
B.100 mL0.1 mol/LFeCl3溶液
C.标准状况下,4.48LHC1气体溶于水配成的1 L溶液
D.向1 L0.2 mol/L BaCl2溶液中加入0.2 mol/L的H2SO4溶液到沉淀恰好完全时的溶液(忽略溶液混合时的体积变化)
【答案】B
【解析】
试题分析:A.300 mL0.1 mol/L NaCl溶液中C1-的物质的量浓度为1×0.1 mol/L=0.1 mol/L;B.100 mL0.1 mol/LFeCl3溶液中C1-的物质的量浓度为3×0.1 mol/L=0.3 mol/L;C.标准状况下,4.48LHC1气体的物质的量为0.2mol,溶于水配成的1 L溶液中C1-的物质的量浓度![]() =0.2mol/L;D.向1 L0.2 mol/L BaCl2溶液中含有氯离子的物质的量为1 L×0.2 mol/L×2=0.4mol,加入0.2 mol/L的H2SO4溶液到沉淀恰好完全时的溶液的体积为2L,其中C1-的物质的量浓度为
=0.2mol/L;D.向1 L0.2 mol/L BaCl2溶液中含有氯离子的物质的量为1 L×0.2 mol/L×2=0.4mol,加入0.2 mol/L的H2SO4溶液到沉淀恰好完全时的溶液的体积为2L,其中C1-的物质的量浓度为![]() =0.2 mol/L;故选B。
=0.2 mol/L;故选B。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.物质的量是一个新的物理量,它表示的是物质的质量
B.周一上午升旗仪式时,学生和老师的物质的量共有2mol
C.物质的量的单位是摩尔,简称摩,用mol表示
D.水的摩尔质量是18g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得1 mol H2与1 mol Cl2反应生成2 mol HCl时,放出184.6 kJ的热量,其理论分析数据与实验数据略有差异,下图表示上述反应能量变化的理论分析示意图:

(1)化学键断裂需要________(填“释放”或“吸收”)能量;
(2)图中化学键形成时共释放能量________kJ;
(3)该反应的反应物的总能量______________(填“大于”“等于”或“小于”)反应产物的能量,所以该反应是______________反应;
(4)用图示数据计算其反应热,写出该反应的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式为:
(1)C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
(2)CH3 COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH2=-870.3 kJ/mol
(3)H2(g)+![]() O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热(ΔH )为
A.+488.3 kJ/mol B.-488.3 kJ/mol
C.- 244.15 kJ/mol D.+244.15 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨在工农业生产中应用广泛。
(1)根据图写出合成氨的热化学方程式是_______________________________。
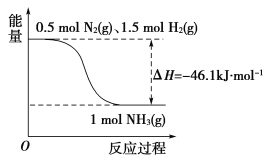
(2)将1 mol N2(g)和3 mol H2(g)放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量________(填“大于”、“等于”或“小于”)92.2 kJ,原因是________________________;若加入催化剂,ΔH________(填“变大”、“不变”或“变小”)。
(3)已知分别破坏1 mol NN键、1 mol HH键时需要吸收的能量为946 kJ、436 kJ,则破坏1 mol NH键需要吸收的能量为________ kJ。
(4)N2H4可视为NH3分子中的H被—NH2取代的产物。发射卫星时以N2H4(g)为燃料、NO2为氧化剂,二者反应生成N2和H2O(g)。
已知:N2(g)+2O2(g)==2NO2(g)
ΔH1=+67.7 kJ·mol-1
N2H4(g)+O2(g)==N2(g)+2H2O(g)
ΔH2=-534 kJ·mol-1
则1 mol N2H4与NO2完全反应的热化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在298K、101kPa时,已知:2H2O(g)=O2(g)+2H2(g) △H1
Cl2(g)+H2(g)=2HCl(g) △H2;
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3
则△H3与△H1和△H2间的关系正确的是( )
A.△H3=△H1+2△H2 B.△H3=△H1+△H2
C.△H3=△H1—2△H2 D.△H3=△H1—△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用地壳中某主要元素生产的多种产品在现代高科技中占有重要位置,足见化学对现代物质文明的重要作用。例如:计算机芯片的主要成分是 ;光导纤维的主要成分是 ;过氧化钠在呼吸面具或潜水艇中作为氧气的来源,其CO2反应的化学方程式为 ;红热的铁跟水蒸气反应,反应的化学方程式为 ;工业上用电解氯化钠溶液的方式制取氯气,反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时c(CO2) 随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
A.该反应的ΔH>0、ΔS<0
B.体系的总压强p:p(Ⅰ)>p(Ⅲ)
C.平衡常数:K(Ⅰ)>K(Ⅱ)
D.T1K时,Ⅳ点所处的状态中v(正)<v(逆)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com