
| A.m×50×18×6.02×1023 |
B. ×6.02×1023 ×6.02×1023 |
C. ×6.02×1023 ×6.02×1023 |
D.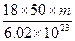 |
科目:高中化学 来源:不详 题型:实验题

| | 是否正确 | 简述理由 |
| 学生甲的观点 | | |
| 学生乙的观点 | | |
| 学生丙的观点 | | |
A. |
B. |
C. |
D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
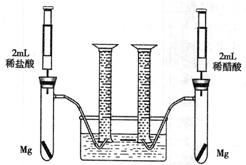
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
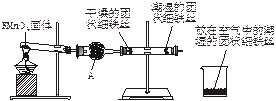
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
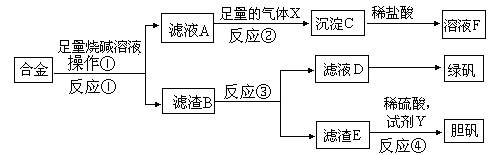
| 实验编号 | 坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 |
| 1 | 11.2g | 25.1g | 19.2g |
| 2 | 11.2g | 25.1g | 18.8g |
| 3 | 11.2g | 25.1g | 18.9g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
|
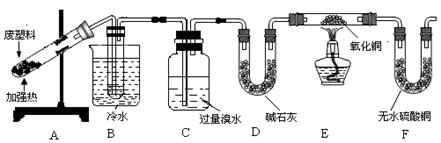
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
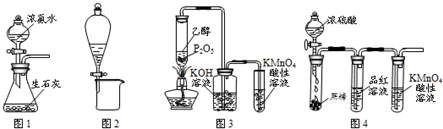
| A.用图1所示装置可制取氨气 |
| B.用图2所示装置可分离CH3CH2OH和CH3COOC2H5混合液 |
| C.用图3所示装置可制取乙烯并验证其易被氧化 |
| D.用图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com