
����Ŀ���ҹ�ij�����Ŷ������̿���Ҫ�ɷ���MnO2������SiO2��Fe2O3���������ʣ�Ϊ��Ҫԭ�ϣ���ȡ�ߴ�̼���̣�������������ͼ:
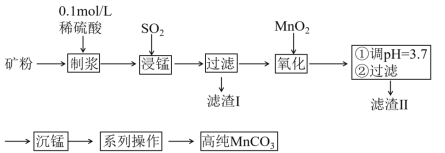
��1���Կ�ʯ���з۴��Ŀ����_______��
��2��������ֱ�Ϊ________��________��
��3������1��ϡ�����������ˮ��Ͽ���ƽ���ԭ����_________�������ý�ŨH2SO4��ԭ����______����ֱ�Ӳ���H2SO4���̵�ԭ����___________��
��4�����̵����ӷ���ʽΪ____________��
��5����ϵ�в�����Ϊ���ˡ�_________�����
��6��ȡ���õĸߴ�MnCO311.7g���������������У���������������������Ba��OH��2Ũ��Һ���գ��õ���ɫ����19.7g�������ò�Ʒ�Ĵ���Ϊ________��������һλС����
���𰸡��ӿ��ȡ���ʣ����ʯ�߽����� SiO2���������裩 Fe��OH��3������������ ���Fe2O3��MnO2�������ԣ����ڱ�SO2��ԭ�ܳ���������������ɣ� �ή��SO2����Һ�е��ܽ�ȣ��Ӷ����ͷ�Ӧ���� MnO2������H2SO4ֱ�ӷ�Ӧ��������������ɣ� MnO2+SO2=Mn2++SO42-��Fe2O3+SO2+2H+=2Fe2++SO42-+H2O ϴ�� 98.3
��������
���̿��ȼ�ϡ�����ƽ���Ȼ��ͨ��SO2�����Ի�����Fe2O3��MnO2��SO2��������������ԭ��Fe2+��Mn2+�����˵õ�������I��ҪΪSiO2����Һ����ҪΪFe2+��Mn2+������MnO2���������������������ӣ�Ȼ�����pH�õ���������������������II������ʱ�ɼ��������̼�����Σ��õ�̼���̳����������ˡ�ϴ�ӡ�����õ��ߴ�̼���̡�
(1)����������Ӵ�������ӿ��ȡ���ʣ����ʯ�߽����ʣ�
(2)���ݷ�����֪����IΪSiO2(��������)������IIΪFe(OH)3(��������)��
(3)����1��ϡ�����������ˮ��Ͽ���ƽ������Ի����������Fe2O3��MnO2�������ԣ����ڱ�SO2��ԭ�ܳ�����ŨH2SO4�ή��SO2����Һ�е��ܽ�ȣ��Ӷ����ͷ�Ӧ���ʣ�MnO2������H2SO4ֱ�ӷ�Ӧ�����Բ�ֱ�Ӳ���H2SO4���̣�
(4)����ʱ���Ի�����Fe2O3��MnO2��SO2���������ӷ���ʽΪ��MnO2+SO2=Mn2++SO42-��Fe2O3+SO2+2H+=2Fe2++SO42-+H2O��
(5)���̵õ�̼���̳����������ˡ�ϴ�ӡ�����õ��ߴ�̼���̣�
(6)̼��������ϡ�������ɵ�����Ϊ������̼��������̼ͨ��������Ba(OH)2Ũ��Һ�õ�����BaCO3����������n(BaCO3)=![]() =0.1mol������̼Ԫ���غ��֪��Ʒ��n(MnCO3)=0.1mol�����Բ�Ʒ����Ϊ
=0.1mol������̼Ԫ���غ��֪��Ʒ��n(MnCO3)=0.1mol�����Բ�Ʒ����Ϊ![]() =98.3%��
=98.3%��


 �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ������ѧ��������λ��������ӵ�صĿ�ѧ�ҡ�ij��������ӵ�صķ�Ӧ����ʽΪLi1-xCoO2+LixC6![]() LiCoO2+C6(x<l)���Ը�����ӵ��Ϊ��Դ������ͪΪԭ���Ʊ������ᣬ����ԭ����ͼ��ʾ��ע�����ữ����ı������ο������������ᣩ��
LiCoO2+C6(x<l)���Ը�����ӵ��Ϊ��Դ������ͪΪԭ���Ʊ������ᣬ����ԭ����ͼ��ʾ��ע�����ữ����ı������ο������������ᣩ��
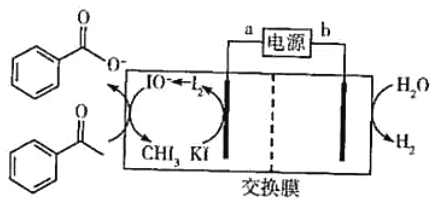
����˵����ȷ���ǣ� ��
A.����ӵ�ص�a��Ϊ����
B.�ŵ�ʱ��������ӦʽΪxLi++xe-+Li1-xCoO2=LiCoO2
C.����ĤΪ���ӽ���Ĥ
D.ÿ����4.48LH2(��״����������0.4molIO-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ��������Ҫ�Ľ���Ԫ��֮һ���䲻���Ǹ��ֲָĵ���Ҫ�ɷ֣��ܶຬ��������Ҳ������Ҫ���塣
��1�����յ����Ų����ɰ�Ԫ�����ڱ��е�Ԫ�ػ��ֳ����������Ԫ������_________����
��2��Mn2+��ˮ��Һ���ѱ���������Fe2+���ױ�����ΪFe3+ ��������ӵļ۵���ʽ�ǶȽ���Mn2+��Fe2+��ԭ�����IJ��_________��Mn2+�İ뾶_________ Fe3+�İ뾶������������������������������
��3����������������ԭ�Ӳ������������ѻ�����������Ŀռ�������Ϊ_________���ú�����ʽ�ӱ�ʾ����
��4����Fe3+����Һ�еμ�������KSCN��Һ����Һ�����ɺ�ɫ��[Fe��SCN����H2O��5]2+��N��H��O����Ԫ�صĵ縺���ɴ�С��˳��Ϊ_________��[Fe��SCN����H2O��5]2+��Fe3+����λ��Ϊ_________��H2O����ԭ�ӵ��ӻ���ʽΪ_________��
��5����ï����һ�ֺ������л�������仯ѧʽΪFe��C5H5��2���ɿ�����Fe2+����������������εĻ����ϩ�����ӣ�C5H![]() �������γɵļ����ͷ��ӣ�����ͼa��ʾ������֪���������÷�����
�������γɵļ����ͷ��ӣ�����ͼa��ʾ������֪���������÷�����![]() ��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ��������籽�����еĴ������ɱ�ʾΪ��������C5H
��ʾ������m���������γɴ�������ԭ������n���������γɴ������ĵ��������籽�����еĴ������ɱ�ʾΪ��������C5H![]() �Ĵ�������ʾΪ________����ï���ǻ�ɫ��״���壬�۵�173 �棨��100 ��ʱ��ʼ���������е�249 �棬��ˮ�����ܣ��������ںܶ��л��ܼ�������������У���ï�������в����ڵ���________�����ţ���
�Ĵ�������ʾΪ________����ï���ǻ�ɫ��״���壬�۵�173 �棨��100 ��ʱ��ʼ���������е�249 �棬��ˮ�����ܣ��������ںܶ��л��ܼ�������������У���ï�������в����ڵ���________�����ţ���
A ���Ӽ� B ��λ�� C �� �� D ���»���
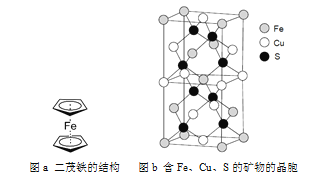
��6��һ�ֺ���Fe��Cu��S����Ԫ�صĿ���ľ���������ͼb��ʾ���������ķ���ϵ����������Ϊ�����Σ���������Sԭ��λ���ڲ���Feԭ��λ�����ĺ;������棬Cuԭ��λ�ھ������档�˿���Ļ�ѧʽΪ_________���������ĵ���߳�ΪA pm����ΪC pm������٤������ΪNA����þ�����ܶ�Ϊ__________ g/cm3��д������ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Journal of Energy Chemistry�������ҹ���ѧ����ƶ�����̼���β��绯ѧת��װ�ã���ʾ��ͼ���£�

����˵������ȷ����
A.cΪ��Դ�ĸ���
B.a���ĵ缫��ӦʽΪ��2C2O52- -4e- =4CO2 ��+O2��
C.�٢��У�����CO2ʱ̼Ԫ�صĻ��ϼ۾�δ�����仯
D.ת��l mol���ӿɲ���CO2 11.2 L(�����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ԫ�صĵ縺�Ժ�ԭ�Ӱ뾶һ����Ҳ��Ԫ�صĻ������ʡ��±�����14��Ԫ�صĵ縺�ԣ�
Ԫ�� | AL | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
�縺�� | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
�Խ��Ԫ�����������֪ʶ����������⡣
(1)�����ϱ����������ݣ�����֪Ԫ�صĵ縺�Ծ��еı仯������__________ (�ӵ縺����ṹ�Ĺ�ϵ����)��
(2)��Ԥ��Br��IԪ�ص縺�ԵĴ�С��ϵ��_________ ��
(3)������ɸ������ǣ����ɼ�����ԭ����ӦԪ�صĵ縺�Բ�ֵ����1.7ʱ��һ��Ϊ���Ӽ�����С��1.7ʱ��һ��Ϊ���ۼ������ƶ�![]() �л�ѧ���������� ___________
�л�ѧ���������� ___________
(4)Ԥ��Ԫ�����ڱ��е縺����С��Ԫ����_____ (������Ԫ�س���)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�����Ȼ�ѧ����ʽ��
Zn(s)��![]() O2(g)=ZnO(s) ��H1=-351.1kJ��mol-1
O2(g)=ZnO(s) ��H1=-351.1kJ��mol-1
Hg(l)��![]() O2(g)=HgO(s) ��H2=-90.7kJ��mol-1
O2(g)=HgO(s) ��H2=-90.7kJ��mol-1
�ɴ˿�֪Zn(s)��HgO(s)=ZnO(s)��Hg(l) ��H3��������H3��ֵ�ǣ� ��
A.-441.8kJ��mol-1B.-254.6kJ��mol-1
C.-438.9kJ��mol-1D.-260.4kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪w gҺ̬��(C6H6)��ȫȼ������2 mol CO2�����1 molҺ̬ˮ�����ų�m kJ����������������ȷ��ʾ��ȼ���ȵ��Ȼ�ѧ����ʽ����(����)
A. 2C6H6(l)��15O2(g)===12CO2(g)��6H2O(l)����H����2m kJ��mol��1
B. ![]() C6H6(l)��
C6H6(l)��![]() O2(g)===2CO2(g)��H2O(l)����H����m kJ��mol��1
O2(g)===2CO2(g)��H2O(l)����H����m kJ��mol��1
C. C6H6(l)��![]() O2(g)===6CO2(g)��3H2O(l)����H����m kJ��mol��1
O2(g)===6CO2(g)��3H2O(l)����H����m kJ��mol��1
D. C6H6(l)��![]() O2(g)===6CO2(g)��3H2O(l)����H����3m kJ��mol��1
O2(g)===6CO2(g)��3H2O(l)����H����3m kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��K����_____________���ܼ����÷��ű�ʾΪ_____________��L����_____________��Ŀ�Լ����÷��ű�ʾΪ_____________��M����_____________���ܼ����÷��ű�ʾΪ_____________���ɴ˿���֪��n(nΪ������)���Ӳ���������_____________���ܼ�����![]() ʱ��������͵������ܼ��ķ��ŷֱ�Ϊ_____________�����ǵ�ԭ�ӹ����״�ֱ�Ϊ_____________��_____________��
ʱ��������͵������ܼ��ķ��ŷֱ�Ϊ_____________�����ǵ�ԭ�ӹ����״�ֱ�Ϊ_____________��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A��ȫȼ��ֻ����CO2��H2O����12g���л�����ȫȼ�յIJ���ͨ������Ũ���ᣬŨ��������14.4g����ͨ��������ʯ�ң���ʯ������26.4g�����л���ķ���ʽ�ǣ� ��
A.C4H10B.C3H8OC.C2H6OD.C2H4O2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com