
【题目】(1)下列物质中,属于强电解质的是(填序号,下同)__________,属于弱电解质的是________,属于非电解质_____________;
①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥氯化银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵 ⑩氢气
(2)硝酸铅的稀溶液中,滴入几滴稀Na2SO4生成白色PbSO4沉淀,再滴入数滴饱和醋酸钠溶液,微热,并不断搅动,沉淀慢慢溶解;请写出沉淀溶解过程的离子方程式_____________;
(3)已知25℃时,H2C2O4的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;H3PO4的电离平衡常数为 K1=7.52×10-3 ,K2=6.23×10-8, K3=2.2×10-13。请写出少量H3PO4与过量Na2C2O4反应的离子方程式:__________________________。
【答案】(1)⑤⑥⑦⑨ ;④ ;①⑧;
(2)PbSO4+2CH3COO-= Pb(CH3COO)2+ SO42—
(3)![]()
【解析】
试题分析:(1)强电解质包括强酸、强碱和绝大多数盐,属于强电解质的是⑤⑥⑦⑨;弱电解质包括弱酸、弱碱、极少数盐和水,属于弱电解质的是④,化合物分为电解质和非电解质,属于非电解质①⑧。
(2)根据题意知PbSO4与饱和醋酸钠溶液发生复分解反应,根据复分解反应发生的条件知醋酸铅为弱电解质,故沉淀溶解过程的离子方程式PbSO4+2CH3COO-= Pb(CH3COO)2+ SO42—。
(3)25℃时,H2C2O4的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;H3PO4的电离平衡常数为 K1=7.52×10-3 ,K2=6.23×10-8, K3=2.2×10-13。则酸性:H2C2O4>H3PO4>HC2O4—>H2PO4—>HPO42—,则少量H3PO4与过量Na2C2O4反应的离子方程式为![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某二元弱酸(简写为H2A)溶液,按下式发生一级或二级电离:
H2A![]() H++HA—;
H++HA—;
HA—![]() H++A2—;
H++A2—;
已知同温同浓度时的电离平衡常数K(H2A)远大于K(HA—),设有下列四种溶液体系:
A. 0.01 mol/L的H2A溶液
B. 0.01 mol/L的NaHA溶液
C. 0.02 mol/L的盐酸与0.04 mol/L的NaHA溶液等体积混合液
D. 0.02 mol/L的氢氧化钠溶液与0.02 mol/L的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1)H+浓度最大的是 ,最小的是 。
(2)H2A浓度最大的是 ,最小的是 。
(3)A2— 浓度最大的是 ,最小的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学设计了如图装置,根据元素非金属性与对应最高价含氧酸之间的关系,可以一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图装置来验证卤族元素性质的递变规律。A、B、C三处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、蘸有碱液的棉花。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
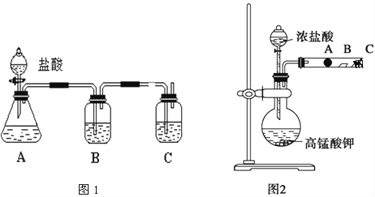
(1)甲同学设计实验的理论依据是_____________________________________;
写出选用药品分别为:A____________,B__________,C____________;
其中装置B中所盛试剂的作用为_____________________________________;
C中反应的离子方程式为____________________________________________;
(2)乙同学的实验理论依据是______________________________________;
A处的现象是: ___________________________________________;
写出B处的离子方程式_____________,C处药品的作用 ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体 g
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
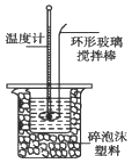
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol): 。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H= (取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是: (填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应mX(g)+nY(g)![]() qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A. 通入稀有气体使压强增大,平衡将正向移动
B. 增加X的物质的量,Y的转化率降低
C. 降低温度,混合气体的平均相对分子质量变小
D. X的正反应速率是Y的逆反应速率的m/n倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一包白色固体,可能含有Na2CO3、NaHCO3和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是
A. 取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一定含有Na2CO3
B. 取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成,说明原固体中一定含有Na2CO3
C. 取一定量固体,溶解,向溶液中滴加适量AgNO3溶液,观察到有白色沉淀生成,说明原固体中一定含有NaCl
D. 称取3.80g固体,加热至恒重,质量减少了0.620g。用足量稀盐酸溶解残留固体,充分反应后,收集到0.880g气体,说明原固体中仅含有Na2CO3和NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达到平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.恒温下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O![]() CO2+H2
CO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com