
【题目】某小组模拟工业上回收分银渣中的银,过程如下:

(1)Na2SO3溶液和氨水均可作浸出剂,但由于氨水易______(填物理性质),故用Na2SO3溶液更环保。
(2)Ⅰ中主要反应:AgCl + 2![]()
![]()
![]() + Cl-。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是______(用离子方程式表示)。
+ Cl-。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是______(用离子方程式表示)。
(3)研究发现:浸出液中含银化合物总浓度与含硫化合物总浓度及浸出液pH的关系如下图。

①pH=10时,含银化合物总浓度随含硫化合物总浓度的变化趋势是______。
②解释①中变化趋势的原因:______。
③pH=5时,含银化合物总浓度随含硫化合物总浓度的变化与pH=10时不同,原因是___。
(4)将Ⅱ中反应的离子方程式补充完整:
□__![]() +□___OH- +□______ = □______ +□______ +□______ + CO32-
+□___OH- +□______ = □______ +□______ +□______ + CO32-
(5)Ⅲ中回收液可直接循环使用,但循环多次后,银的浸出率会降低。从回收液离子浓度变化和反应限度的角度分析原因:______。
【答案】挥发 2![]() 含银化合物总浓度随含硫化合物总浓度的增大而增大 浸出液中c(
含银化合物总浓度随含硫化合物总浓度的增大而增大 浸出液中c(![]() )增大,使浸出反应的平衡正向移动 pH较小时,
)增大,使浸出反应的平衡正向移动 pH较小时,![]() 与H+结合生成
与H+结合生成![]() 或H2SO3,尽管含硫化合物总浓度增大,但c(
或H2SO3,尽管含硫化合物总浓度增大,但c(![]() )均较小 4 6 HCHO 4Ag 8
)均较小 4 6 HCHO 4Ag 8![]() 4H2O 随着循环次数增加,浸出液中c(
4H2O 随着循环次数增加,浸出液中c(![]() )减小、c(Cl-)增大,均使AgCl + 2
)减小、c(Cl-)增大,均使AgCl + 2![]()
![]()
![]() + Cl-的限度减小
+ Cl-的限度减小
【解析】
分银渣中主要成分是AgCl,Ⅰ中用Na2SO3溶液作浸出剂,主要反应:AgCl + 2![]()
![]()
![]() + Cl-;浸出液与甲醛反应,Ⅱ中发生4
+ Cl-;浸出液与甲醛反应,Ⅱ中发生4![]() +6OH-+HCHO=4Ag+8
+6OH-+HCHO=4Ag+8![]() +4H2O+
+4H2O+![]() 反应,生成Ag回收,同时又生成
反应,生成Ag回收,同时又生成![]() ,III中循环使用。
,III中循环使用。
(1)氨水易挥发污染空气,故用Na2SO3溶液更环保;
(2)反应在敞口容器中进行,![]() 很容易被空气中氧气氧化,离子反应方程式为2
很容易被空气中氧气氧化,离子反应方程式为2![]() ;
;
(3)①根据图像可知,当pH=10时,含银化合物总浓度随含硫化合物总浓度的增大而增大;
②①中变化趋势的原因:浸出液中c(![]() )增大,使浸出反应AgCl + 2
)增大,使浸出反应AgCl + 2![]()
![]()
![]() + Cl-的平衡正向移动;
+ Cl-的平衡正向移动;
③ pH=5时,含银化合物总浓度随含硫化合物总浓度的变化与pH=10时不同,pH较小时,![]() 与H+结合生成
与H+结合生成![]() 或H2SO3,尽管含硫化合物总浓度增大,但c(
或H2SO3,尽管含硫化合物总浓度增大,但c(![]() )均较小;
)均较小;
(4)Ag的化合价由+1价降至0价,HCHO被氧化成CO32-,回收液循环使用,说明有SO32-生成,根据得失电子守恒、电荷守恒和原子守恒配平得:4![]() +6OH-+HCHO=4Ag+8
+6OH-+HCHO=4Ag+8![]() +4H2O+
+4H2O+![]()
(5)随着循环次数增加,浸出液中c(![]() )减小、c(Cl-)增大,均使AgCl + 2
)减小、c(Cl-)增大,均使AgCl + 2![]()
![]()
![]() + Cl-的限度减小
+ Cl-的限度减小


科目:高中化学 来源: 题型:
【题目】感冒是一种常见的病,病人患了感冒会咳嗽、流涕、发烧,多喝开水多休息,适当服用一些治疗感冒的药,可以舒缓症状,减轻病情。药物阿司匹林是一种传统的治疗感冒发烧的药,从分子结构上看,它可以看做是乙酸酯,其结构简式为
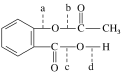
(1)阿司匹林与NaOH溶液反应中,可以断裂的化学键是________(填代号)。
(2)根据阿司匹林的结构推断它能够发生的化学反应类型为________(填序号)。
①中和反应 ②加成反应 ③取代反应
(3)阿司匹林连接在某高分子聚合物上,可形成缓解长效药物,其中的一种结构为
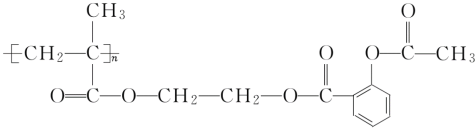
则缓释长效阿司匹林载体的结构简式为_______。
(4)长期大量服用阿司匹林会出现不良反应,一旦出现水杨酸中毒现象,应立即停药,并静脉滴注NaHCO3溶液,以解除水杨酸的中毒症状,反应的化学方程式为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5有机化合物】甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。

已知:
请回答:
(1)写出下列反应方程式
①B+D→E______________________________________。
②G→H________________________________________。
(2)①的反应类型为__________;②的反应类型为__________;F的结构简式为__________。
(3)E、J有多种同分异构体,写出符合下列条件的4种同分异构体的结构简式。要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
__________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参照反应Br+H2→HBr+H的能量随反应历程变化的示意图,下列叙述中正确的是
A. 反应物具有的总能量大于生成物具有的总能量
B. 正反应为吸热反应
C. 该反应的逆反应是吸热过程
D. 图中可以看出,HBr的能量一定高于H2的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火柴头中含有Cl元素的证明,有同学设计了以下实验流程图:

(1)实验中发生的离子反应是______________________
(2)有人提出上述方法中出现白色沉淀并不能充分说明火柴头上 KClO3的存在,其理由是________。如何解决这个问题____________
(3)实验测得火柴头中KClO3的质量分数为____________;未洗涤沉淀,测得KClO3的质量分数将_________(填 “偏大”、“偏小”、或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛分子的结构式如图所示,下列描述正确的是( )
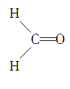
A. 甲醛分子中有4个σ键
B. 甲醛分子中的C原子为sp3杂化
C. 甲醛分子中的O原子为sp杂化
D. 甲醛分子为平面三角形,有一个π键垂直于三角形平面
查看答案和解析>>
科目:高中化学 来源: 题型:
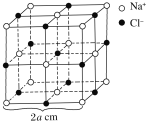
【题目】如图为NaCl晶体的一个晶胞,测知氯化钠晶体中相邻的Na+与Cl-的距离为a cm,该晶体密度为d g·cm-3,则阿伏加德罗常数可表示为多少________________________(书写计算的步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2![]() 2Cl2+2H2O
2Cl2+2H2O
已知:反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
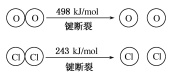
(1)H2O的电子式是________。
(2)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为________kJ;H2O中H—O键比HCl中H—Cl键________(填“强”或“弱”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是温度和压强对X+Y![]() 2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
2Z反应影响的示意图。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )
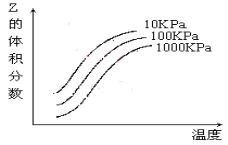
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中只有一种是气态,Z为气态
D.上述反应的逆反应的△H>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com