
【题目】火柴头中含有Cl元素的证明,有同学设计了以下实验流程图:

(1)实验中发生的离子反应是______________________
(2)有人提出上述方法中出现白色沉淀并不能充分说明火柴头上 KClO3的存在,其理由是________。如何解决这个问题____________
(3)实验测得火柴头中KClO3的质量分数为____________;未洗涤沉淀,测得KClO3的质量分数将_________(填 “偏大”、“偏小”、或“无影响”)。
【答案】ClO3- + 3NO2- + Ag+ = AgCl↓+ 3NO3- AgNO2与AgCl均为不溶于水的白色沉淀 加稀硝酸酸化 50% 偏大
【解析】
火柴头是由氯酸钾KClO3,二氧化锰MnO2,三硫化二锑Sb2S3,硫S组成的,用来擦燃火柴的纸是由P(红磷)做成的。火柴头用水浸泡,KClO3会溶于水中。KClO3具有氧化性,能够与NaNO2发生氧化还原反应,,其中Cl的化合价降低得到Cl-,Cl-与Ag+结合生成AgCl。
(1)ClO3-和NO2-发生氧化还原反应,其中Cl的化合价降低生成Cl-,Cl-再和Ag+反应生成AgCl,则离子方程式为ClO3- + 3NO2- + Ag+ = AgCl↓+ 3NO3-;
(2)因为加入了NaNO2,而Ag+也可与NO2-反应生成AgNO2沉淀,也是白色的,与AgCl不能区分;而AgNO2会溶于HNO3,而AgCl不溶于HNO3,因此可以加入稀硝酸酸化,答案为AgNO2与AgCl均为不溶于水的白色沉淀 加稀硝酸酸化;
(3)得到的白色沉淀为AgCl,其质量为1.435g,其物质的量为1.435g÷143.5g·mol-1=0.01mol,根据氯守恒,则KClO3的物质的量为0.01mol,其质量为0.01mol×122.5g·mol-1=1.225g,则KClO3的质量分数为1.225g÷2.45g×100%=50%。如果没有洗涤,得到的AgCl的质量偏大,则测得KClO3的质量分数偏大。


科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是![]() ,含
,含![]() 、
、![]() 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下:
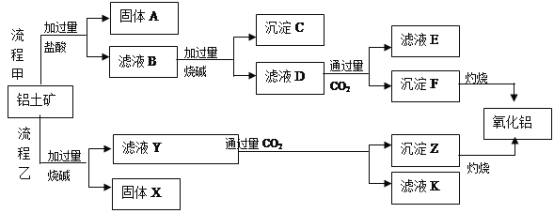
请回答下列问题:
(1)流程乙加入烧碱后的离子方程式为_________________________________________.
(2)固体A的应用_________________________________________.(两点)
(3)滤液D与少量CO2反应的离子方程式为__________________________________,
向该滤液K中加入足量石灰水的离子方程式是________
(4)流程乙制氧化铝的优点是所用的试剂较经济,缺点是__________________________
(5)已知298K时,![]() 的溶度积常数
的溶度积常数![]() =10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为_______.
=10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的pH最小为_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4。其反应的离子方程式:Fe(OH)3+ClO-+OH-→FeO42-+H2O+Cl-(未配平)。配平上述离子方程式,用单线桥法标出电子转移方向和数目。___
___Fe(OH)3+___ClO-+___OH-→___FeO42-+___H2O+___Cl-
该反应中,还原剂是___,被还原的元素是___。
(2)在一定温度下,氧化铁可以与一氧化碳发生反应:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)+Q。
2Fe(s)+3CO2(g)+Q。
已知该反应在不同温度下的平衡常数如表。
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 64.0 | 50.7 | 42.9 |
该反应的平衡常数表达式为___,Q__0(填“>”、“<”或“=”)。
(3)在容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡,该时间范围内反应的平均反应速率v(CO2)=___,CO的平衡转化率为____。
(4)欲提高CO的平衡转化率,可采取的措施是___。
A.减少Fe的量 B.增加Fe2O3的量
C.移出部分CO2 D.提高反应温度
E.减小容器的容积 F.加入合适的催化剂
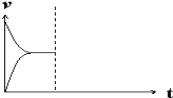
(5)现在恒压密闭容器中通入1molH2和1molCO2发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g)+41kJ。当反应达到平衡后,在其他条件不变时,再通入1molH2和1molCO2的混合气体,请在图中画出正(v正)、逆(v逆)反应速率随时间t变化的示意图。___
CO2(g)+H2(g)+41kJ。当反应达到平衡后,在其他条件不变时,再通入1molH2和1molCO2的混合气体,请在图中画出正(v正)、逆(v逆)反应速率随时间t变化的示意图。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯是一种无毒、无臭的热塑性材料,被广泛应。工业由苯和乙烯为原料制备聚苯乙烯的流程如 下图所示(部分条件略去),下列说法错误的是( )
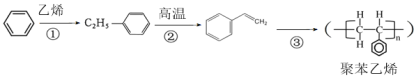
A.过程①生成乙苯,反应类型为加成反应
B.过程②生成苯乙烯,苯乙烯16个原子一定共面
C.过程③原子利用率为100%,反应类型为加聚反应
D.上述流程中涉及的五种有机物均可使溴水或高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在体积均为20mL、浓度均为0.1mol/L的HX溶液、HY溶液中分别滴加0.1mol/L的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加NaOH溶液体积的关系如图所示。下列推断正确的是
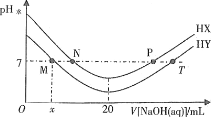
A.HX的电离方程式为HX=H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都一定降低
D.常温下,HY的电离常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组模拟工业上回收分银渣中的银,过程如下:

(1)Na2SO3溶液和氨水均可作浸出剂,但由于氨水易______(填物理性质),故用Na2SO3溶液更环保。
(2)Ⅰ中主要反应:AgCl + 2![]()
![]()
![]() + Cl-。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是______(用离子方程式表示)。
+ Cl-。研究发现:其他条件不变时,该反应在敞口容器中进行,浸出时间过长会使银的浸出率(浸出液中银的质量占起始分银渣中银的质量的百分比)降低,可能原因是______(用离子方程式表示)。
(3)研究发现:浸出液中含银化合物总浓度与含硫化合物总浓度及浸出液pH的关系如下图。

①pH=10时,含银化合物总浓度随含硫化合物总浓度的变化趋势是______。
②解释①中变化趋势的原因:______。
③pH=5时,含银化合物总浓度随含硫化合物总浓度的变化与pH=10时不同,原因是___。
(4)将Ⅱ中反应的离子方程式补充完整:
□__![]() +□___OH- +□______ = □______ +□______ +□______ + CO32-
+□___OH- +□______ = □______ +□______ +□______ + CO32-
(5)Ⅲ中回收液可直接循环使用,但循环多次后,银的浸出率会降低。从回收液离子浓度变化和反应限度的角度分析原因:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用铜萃取剂M,通过如下反应实现铜离子的富集:

(1)X难溶于水、易溶于有机溶剂,其晶体类型为________。
(2)M所含元素的电负性由大到小顺序为_______,N原子以_____轨道与O原子形成σ键。
(3)上述反应中断裂和生成的化学键有______(填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是_____。

(5)基态Cu2+的外围电子排布式为________,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是___________。
离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是前20号元素中的部分元素的一些数据:
A | B | C | D | E | F | G | H | I | J | |
原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
试回答下列问题:
(1)以上10种元素电负性最大的是_____(填元素符号)。比元素B原子序数大7的元素在元素周期表中的位置:第_____周期,第_____族,其基态原子的核外电子排布式是________。
(2)H、I、J三种元素对应单质的熔点依次升高的顺序是(用单质的具体化学式排序)__________。
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子。其分子中共形成________个σ键,________个π键。
(4)I与氢元素形成的10电子分子X的空间构型为________;将X溶于水后的溶液滴入到CuSO4溶液中至过量,得到的络离子的化学式为________,其中X与Cu2+之间以_____________键结合。
(5)下图是I元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:
a._________________________________。
b._________________________________。
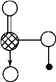
(6) 如图是J和E组成的晶体结构,则每个与J周围最近J原子数目为_________,若晶胞边长为a cm,则晶体的密度为_______________(用含a、NA的代数式表示)(g/mL)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
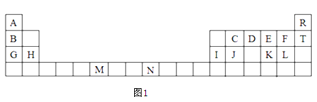
试回答下列问题:
(1)F-的结构示意图:__。
(2)D的气态氢化物的VSEPR模型为___,其中心原子的杂化类型为___,分子的空间构型为___。
(3)G、H和I的第一电离能数值由大到小的顺序为:___(用元素符号作答)。
(4)元素M的化合物(MO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
①与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有____(填元素符号)。
②MO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断MO2Cl2是___(填“极性”或“非极性”)分子。
③在C2H4、CH3Cl、CH2O、CS2、CCl4五种有机化合物中,碳原子采取sp2杂化的分子有___(填分子式)。
(5)已知元素N可形成一种红紫色配合物,其组成为NCl3·5NH3·H2O。该配合物中的中心离子N离子在基态时核外简化电子排布式为___,又已知中心离子N离子的配位数是6,1mol该物质与足量的硝酸银反应可生成3molAgCl,则该物质的配体是___。
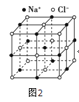
(6)过去常以JE2为催化剂的载体。JE2的晶胞可作如下推导:先将NaCl晶胞中的所有Na+去掉,并将Cl-全部换成J原子,再在每两个不共面的“小立方体”中心处各放置一个J原子便构成了晶体J的一个晶胞,则一个J的晶胞中有___个J原子,再在每两个相邻的J原子(距离最近的两个J原子)中心连线的中点处增添一个E原子,便构成了JE2晶胞,故JE2晶胞中有___个E原子。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com