
【题目】氮的固定对工农业及人类生存具有重大意义。
合成氨是最重要的人工固氮:N2(g)+3H2(g) ![]() 2NH3(g) △H<0。
2NH3(g) △H<0。
(1)下列关于该反应的说法中,正确的是___________(填正确选项字母编号)。
A.反应达到平衡状态时,N2、H2、NH3的体积比为1∶3∶2
B.加催化剂可以加快正反应速率,减慢逆反应速率
C.高温既有利于加快反应速率也有利于提高氨气的产率
D.高压既有利于加快反应速率也有利于提高氨气的产率
(2)一定温度下,在容积为1L的密闭容器中,加入lmolN2和3mol H2,反应达到平衡时H2的转化率为60%,此时反应消耗N2物质的量为___________mol;保持容器体积不变,再向容器中加入1molN2,3mol H2,反应再次达到平衡时,氢气的转化率将___________(填“增大”或“减小”或“不变”)。
(3)标准状况下,将22.4 mL的氨气通入100 mL 0.01 mol·L-1的盐酸中,充分反应后,溶液中各离子浓度由大到小的顺序是________________________。
(4)将氨气通入盛有CaSO4悬浊液的沉淀池中,再通入适量的CO2气体,充分反应后,过滤所得滤液为(NH4)2SO4溶液,该过程的化学反应方程式为____________________。
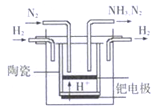
(5)20世纪末,科学家采用高质子导电性的SCY陶瓷(能传递 H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现常压、570℃高温的电解法合成氨,提高了反应物的转化率,其实验简图如图所示,写出阴极的电极反应式____________________。
【答案】 D 2.08 增大 c(Cl-)>c(NH4+)>c(H+)>c(OH-) CaSO4+CO2+2NH3+H2O=CaCO3+(NH4)2SO4 N2+6e-+6H+=2NH3
【解析】(1)A.a.容器内N2、H2、NH3的浓度之比为1:3:2,不能说明达到判断状态,取决于起始配料比和转化程度,故A错误;B.催化剂能同等程度加快正反应和逆反应速率,故B错误;C.高温既有利于加快反应速率,但此时平衡逆向移动,不利于提高氨气的产率,故C错误;D.高压可以加快反应速率,也能促进平衡正向移动,有利于提高氨气的产率,故D正确;答案为D。
(2)根据 N2(g)+3H2(g)2NH3(g)氢气的变化量为1.8mol,则反应消耗N2物质的量为1.8mol×![]() =0.6mol;保持容器体积不变,再向容器中加入lmolN2,3molH2,相当于在2L容器中加入2molN2、6molH2反应达到平衡时再缩小体积到1L,此时平衡正向移动,氢气的转化率增大;
=0.6mol;保持容器体积不变,再向容器中加入lmolN2,3molH2,相当于在2L容器中加入2molN2、6molH2反应达到平衡时再缩小体积到1L,此时平衡正向移动,氢气的转化率增大;
(3)标准状况下,若将22.4mL的氨气通入100mL0.01mol/L的盐酸中得到NH4Cl溶液,NH4+的水解使得溶液显酸性,即c(H+)>c(OH-),再结合溶液中的电荷守恒可知溶液中各离子浓度的顺序由大到小为c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(4)将氨气通入盛有CaSO4悬浊液的沉淀池中,再通入适量的CO2气体,可得到碳酸钙沉淀,同时过滤得滤液为(NH4)2SO4溶液,发生反应的化学方程式为CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4;
(5)电解池中氮气在阴极得电子生成氨气,其电极方程式为:N2+6e-+6H+=2NH3。


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】在空气中,有下列反应发生: ①N2 + O2 = 2NO;②2NO+O2=2NO2;③3NO2 + H2O = 2HNO3 + NO;④ 2SO2+O2 = 2SO3;⑤ SO3 + H2O = H2SO4; ⑥SO2+H2O![]() H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
A. ①②③④ B. ①②③④⑦ C. ①②④⑦ D. ①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100 ℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2![]() N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为_______,混合气体的平均摩尔质量为____________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2![]() N2O4的平衡常数将________(填“增大”“减小”或“不变”)。
N2O4的平衡常数将________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将________(填“向左移动”、“向右移动”或“不移动”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中进行反应C(s)+H2O(g)![]() CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是
CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图。下列判断正确的是

A.0~5min内,v (H2)=0.05mol/(Lmin)
B.5min时该反应的K值一定小于12 min时的K值
C.10 min时,改变的外界条件可能是减小压强
D.5min时该反应的v (正)大于11 min 时的v (逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着工业的发展,大气中CO2的浓度不断增加,如何减少CO2排放已成为全世界关注的热点,低碳经济和低碳生活成为热门话题,以下做法与低碳要求相违背的是 ( )
A.控制高能耗企业上马 B.尽量不使用一次性筷子
C.提倡骑自行车、乘共交车出行 D.多挖煤,多发电,加快经济发展
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施能使氢气生成速率加大的是( )
A. 加少量CH3COONa固体 B. 加硝酸钾固体
C. 不用铁片,改用铁粉 D. 不用稀硫酸,改用98%浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10 L的密闭容器中,A、B、C 三种物质的物质的量(n)与时间(t)的关系如图一所示,C的百分含量(C%)与温度(T)的关系如图二所示,下列分析错误的是( )

A. 该反应的化学方程式是2A+B![]() C
C
B. 0~4 min时,A的平均反应速率为0.1 mol/(L·min)
C. 由T1向T2变化时,v(正)>v(逆)
D. 平衡后升高温度,反应的平衡常数K值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学研究合成氨反应及氨水的性质如下:
(1)已知:N2(g)+3H2(g)=2NH3(g) △H =-92.4 kJ/mol
2H2(g)+O2(g)=2H2O(g) △H =-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式__________________________。
(2)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是_______________(填“温度”或“压强”),判断L1、L2的大小关系:L1______L2(填“<”或“>”)。

(3)已知:在硫酸铜溶液中加入浓氨水,首先析出蓝色的碱式硫酸铜沉淀,氨水过量时此沉淀溶解,得到深蓝色的四氨合铜(Ⅱ)络离子,发生的离子反应如下:
a.2Cu2++ 2NH3·H2O+ SO42-=== 2NH4+ + Cu2(OH)2SO4↓
b.Cu2(OH)2SO4 + 8 NH3![]() 2[Cu(NH3)4]2++SO42-+2 OH-
2[Cu(NH3)4]2++SO42-+2 OH-
某小组设计如下实验:

①试管ⅰ中反应的离子方程式_______________________________________。
②试管ⅱ中的深蓝色晶体是[Cu(NH3)4]SO4·H2O,该实验现象反映出该晶体的性质是______。
③请结合方程式解释试管ⅲ加入少量NaOH后产生蓝色沉淀和气体的原因_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 常温常压下,11.2L二氧化硫所含的氧原子数等于NA
B. 0.5molH2O所含的电子数为9NA
C. 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA
D. 300mL2mol·L-1蔗糖溶液中所含分子数为0.6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com