
【题目】二甲醚(CH3OCH3)是一种重要的清洁燃料气,其储运、燃烧安全性、理论燃烧温度等性能指标均优于液化石油气,也可用作燃烧电池,具有很好的发展前景。
(1)已知 H2、CO 和CH3OCH3的燃烧热(ΔH)分别为-285.5kJ/mol、 -283kJ/mol 和-1460.0kJ/mol,则工业上利用水煤气成分按 1:1 合成二甲醚的热化学方程式为: ____________。
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成 Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的 H2,将悬浮物带到水面,利于除去。实验室以二甲醚燃料电池模拟该方法设计的装置如下图所示:
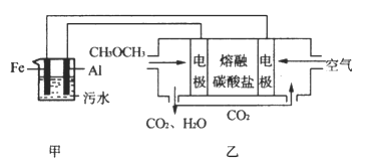
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极。写出该燃料电池的正极电极反应式 __________;下列物质可用做电池熔融碳酸盐的是 ______。
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)2CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式____________________。
③已知常温下 Ksp[Fe(OH)3]=4.0×10-38,电解一段时间后,甲装置中 c(Fe3+)=___________。
④已知:H2S的电离平衡常数: K1=9.1×10-8、 K2=1.1×10-12; H2CO3的电离平衡常数:K1=4.31×10-7、 K2=5.61×10-11。测得电极上转移电子为 0.24mol 时,将乙装置中生成的 CO2通入200mL 0.2mol/L的Na2S溶液中,下列选项正确的是______
A.发生反应的离子方程式为:CO2+S2-+H2O=CO32-+H2S
B.发生反应的离子方程式为: CO2+S2-+H2O=HCO3-+HS-
C.c(Na+)=2[c(H2S)+c(HS-)+c(S2-)
D.c(Na+)+c(H+)=2c(CO32-)+2c(S2-)+c(OH-)
E. c(Na+)>c(HCO3-)>c(HS-)>c(OH-)
【答案】2H2(g)+3CO(g)=CH3OCH3(g)+CO2(g) △H=-246.4 kJ·mol-1 O2+4e-+2CO2=2CO32- B 4Fe2++O2+10H2O=4Fe(OH)3+8H+ 4.0×10-11mol/L B、C、E
【解析】
(1)①H2(g)+![]() O2(g)=H2O(l)△H=-285.5kJ/mol,②CO(g)+
O2(g)=H2O(l)△H=-285.5kJ/mol,②CO(g)+![]() O2(g)=CO2(g)△H=-283kJ/mol,③CH3OCH3(g)+3O2=2CO2(g)+3H2O(l)△H=-1460.0kJ/mol
O2(g)=CO2(g)△H=-283kJ/mol,③CH3OCH3(g)+3O2=2CO2(g)+3H2O(l)△H=-1460.0kJ/mol
用水煤气成分按1:1合成二甲醚,将方程式3①+3②-③得:3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g)△H=3(-285.5kJ/mol)+3(-283kJ/mol)-(-1460.0kJ/mol)=-245.5kJ/mol,故答案为3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g)△H=-245.5kJmol-1;
(2)①燃料电池中,正极上氧化剂氧气得电子和二氧化碳发生还原反应生成碳酸根离子,电极反应式为O2+4e-+2CO2=2CO32-;熔融碳酸盐性质要稳定,高温时不能分解生成其它物质,A.MgCO3高温下分解生成氧化镁和二氧化碳而得不到碳酸根离子,故错误; B.Na2CO3性质较稳定,熔融状态下只发生电离而不发生分解反应,故正确;C.NaHCO3性质不稳定,易分解而得不到碳酸根离子,故错误;D.(NH4)CO3性质不稳定,易分解而得不到碳酸根离子,故错误;故答案为O2+4e-+2CO2=2CO32-;B;
②阳极上Fe失电子生成亚铁离子,阴极上生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,被氧气氧化生成氢氧化铁,离子反应方程式为:4Fe2++O2+10H2O=4Fe(OH)3↓+8H+,故答案为4Fe2++O2+10H2O=4Fe(OH)3↓+8H+;
③c(Fe3+)=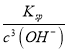 =
= mol/L=4.0×10-11 mol/L,故答案为4.0×10-11mol/L;
mol/L=4.0×10-11 mol/L,故答案为4.0×10-11mol/L;
④乙装置中阴极上甲醚失电子生成二氧化碳,根据CH3OCH3---2CO2---12e-计算n(CO2)=![]() =0.04mol,n(Na2S)=0.2mol/L×0.2L=0.04mol,根据电离平衡常数知发生反应CO2+S2-+H2O═HCO3-+HS-,则溶液中的溶质是等物质的量浓度的NaHCO3、NaHS,A.根据以上分析知,发生反应的离子方程式为:CO2+S2-+H2O═HCO3-+HS-,故错误;B.根据以上分析知,发生反应的离子方程式为:CO2+S2-+H2O═HCO3-+HS-,故正确;C.根据物料守恒得c(Na+)=2[c(H2S)+c(HS-)+c(S2-)],故正确;D.根据电荷守恒得c(Na+)+c(H+)=2c(CO32-)+2c(S2-)+c(OH-)+c(HS-)+c(HCO3
=0.04mol,n(Na2S)=0.2mol/L×0.2L=0.04mol,根据电离平衡常数知发生反应CO2+S2-+H2O═HCO3-+HS-,则溶液中的溶质是等物质的量浓度的NaHCO3、NaHS,A.根据以上分析知,发生反应的离子方程式为:CO2+S2-+H2O═HCO3-+HS-,故错误;B.根据以上分析知,发生反应的离子方程式为:CO2+S2-+H2O═HCO3-+HS-,故正确;C.根据物料守恒得c(Na+)=2[c(H2S)+c(HS-)+c(S2-)],故正确;D.根据电荷守恒得c(Na+)+c(H+)=2c(CO32-)+2c(S2-)+c(OH-)+c(HS-)+c(HCO3


科目:高中化学 来源: 题型:
【题目】实验室用乙酸和乙醇在浓硫酸作用下制取乙酸乙酯的装置如图。下列说法正确的是
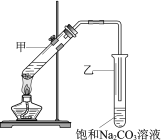
A. 向甲试管中先加浓硫酸,再加乙醇和乙酸
B. 乙试管中导管不伸入液面下,是为了防止倒吸
C. 加入过量乙酸,可使乙醇完全转化为乙酸乙酯
D. 实验完毕,可将乙酸乙酯从混合物中过滤出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z原子序数依次增大,甲、乙、丙、丁、戊、己是由这些元素构成的物质。常温下,丙和戊是单质气体,乙为生活中常见的无色液体,戊能使带火星的木条复燃,0.01mol/L丁溶液pH=12,上述物质的转化关系如图所示.下面说法正确的是
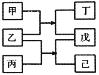
A.原子半径:X<Y<ZB.单质沸点:W>X
C.气态氢化物的热稳定性:X>YD.Y和Z形成的化合物溶于水显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() 为吸热反应,下列对该反应的说法正确的是( )
为吸热反应,下列对该反应的说法正确的是( )
A.X的能量一定低于M的能量,Y的能量一定低于![]() 的能量
的能量
B.因为该反应为吸热反应,故需要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量
D.反应物X和Y的总能量大于生成物M和N的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳氧化物研究
![]() 和
和![]() 在一定条件下可以合成甲醇:
在一定条件下可以合成甲醇:![]() ,现在体积为1L的恒容密闭容器
,现在体积为1L的恒容密闭容器![]() 图甲
图甲![]() 中通入1molCO和
中通入1molCO和![]() ,测定不同时间、不同温度
,测定不同时间、不同温度![]() 下容器中CO的物质的量,如表:
下容器中CO的物质的量,如表:

0min | 10min | 20min | 30min | 40min | |
| 1mol |
|
|
|
|
| 1mol |
|
| a | a |
请回答:
![]() ______
______![]() 填“
填“![]() ”或“
”或“![]() ”或“
”或“![]() ”
”![]() ,理由是______。已知
,理由是______。已知![]() 时,第20min时容器内压强不再改变,此时
时,第20min时容器内压强不再改变,此时![]() 的转化率为______,该温度下的化学平衡常数为______。
的转化率为______,该温度下的化学平衡常数为______。
![]() 若将1molCO和
若将1molCO和![]() 通入原体积为1L的恒压密闭容器
通入原体积为1L的恒压密闭容器![]() 图3乙
图3乙![]() 中,在
中,在![]() 下达到平衡,此时反应的平衡常数为______;若再向容器中通入
下达到平衡,此时反应的平衡常数为______;若再向容器中通入![]() ,重新达到平衡后,
,重新达到平衡后,![]() 在体系中的百分含量______
在体系中的百分含量______![]() 填“变大”或“变小”或“不变”
填“变大”或“变小”或“不变”![]() 。
。
![]() 一定条件下也可用NaOH溶液与CO反应生成甲酸钠,进一步反应生成甲酸来消除CO污染。常温下将amol的CO通入
一定条件下也可用NaOH溶液与CO反应生成甲酸钠,进一步反应生成甲酸来消除CO污染。常温下将amol的CO通入![]() NaOH溶液中,恰好完全反应生成甲酸钠和含少量甲酸的混合溶液
NaOH溶液中,恰好完全反应生成甲酸钠和含少量甲酸的混合溶液![]() 假设溶液体积不变
假设溶液体积不变![]() ,测得溶液中
,测得溶液中![]() ,则该混合溶液中甲酸的电离平衡常数
,则该混合溶液中甲酸的电离平衡常数![]() ______
______![]() 用含a和b的代数式表示
用含a和b的代数式表示![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氢气与氧气反应生成水蒸气的能量变化示意图。下列有关说法不正确的是( )
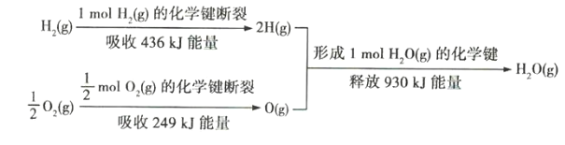
A.反应中断裂和形成的化学键均为共价键
B.该反应过程释放能量
C.断裂1mol液态水中的化学键需吸收930kJ能量
D.2mol O(g)形成1mol O2(g)释放498kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1mol·L-1NaHCO3溶液:Na+、Ba2+、NO3-、OH-
B.0.1mol·L-1NaAlO2溶液:K+、OH-、Cl-、NO3-
C.![]() =1.0×1012的溶液:Fe2+、Mg2+、NO3-、I-
=1.0×1012的溶液:Fe2+、Mg2+、NO3-、I-
D.0.1mol·L-1FeCl3溶液:K+、Cu2+、SCN-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Z具有广谱抗菌活性,可利用X和Y反应获得。下列有关说法正确的是( )
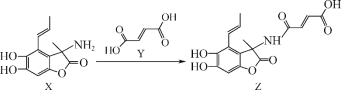
A.有机物X的分子式为C12H13O4N
B.有机物Y可以和乙醇发生缩聚反应
C.有机物Y中所有原子可能在同一平面上
D.1mol有机物Z与足量NaOH溶液反应最多消耗4mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com