
【题目】四甲基氢氧化铵[(CH3)4NOH]常用作电子工业清洗剂,以四甲基氯化铵[(CH3)4NCl]水溶液为原料,通过电解法制备(CH3)4NOH,其工作原理如图所示,下列说法正确的是( )
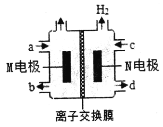
A.M电极的电极反应式为:4OH--4e-=O2↑+2H2O
B.N电极接电源的正极
C.阳离子通过离子交换膜往M电极移动
D.制备18.2g(CH3)4NOH,两极共产生4.48L气体(标准状况)
【答案】D
【解析】
N电极有氢气生成,发生还原反应,故N为阴极,则M为阳极;N极区水放电生成氢气与氢氧根离子,氢氧根离子再与溶液中(CH3)4N+结合生成(CH3)4NOH,M极区是氯离子放电生成氯气,离子交换膜为阳离子交换膜;N极电极反应式为:2(CH3)4N++2H2O+2e=2(CH3)4NOH+H2↑,M极电极反应式为:2Cl2e=Cl2↑。
A.N电极有氢气生成,发生还原反应,故N为阴极,则M为阳极,M极电极反应式为:2Cl2e=Cl2↑,故A错误;
B.N为阴极,连接电源的负极,故B错误;
C.在电解池中,阳离子向阴极移动,N为阴极,所以向N极移动,故C错误;
D.18.2g(CH3)4NOH的物质的量为18.2g÷92g/mol=0.2mol,N极电极反应式为:2(CH3)4N++2H2O+2e=2(CH3)4NOH+H2↑,收集氢气0.1mol,转移电子为0.2mol,M极电极反应式为:2Cl2e=Cl2↑,收集氯气为0.1mol,故标况下两极可得气体体积为:0.2mol×22.4L/mol=4.48L,故D正确;
故答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是( )
A.除去Cl2中含有的少量HCl 
B.蒸干FeCl3饱和溶液制备FeCl3晶体
C.制取少量纯净的CO2气体
D.分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定体积的密闭容器中,加入2mol A和1mol B发生可逆反应2A(g)+B(g)3C(g)+D(g),达到平衡,C的浓度为w mol/L。若维持容器体积和温度不变,下列四种配比作为起始物质,达平衡后,C的浓度仍为w mol/L的是( )
A.4 mol A+2 mol B B.1 mol B+3 mol C+1 mol D
C.3 mol C+2 mol D D.1 mol A+0.5 mol B+1.5 mol C+0.5 mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硝酸锶[Sr(NO3)2]可用于制造信号灯,光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如图:
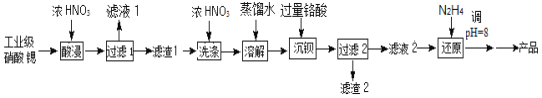
已知:①“滤渣1”的成份为Ba(NO3)2、Sr(NO3)2;②铬酸(H2CrO4)为二元弱酸
(1)用铬酸(H2CrO4)“沉钡”,是工业上常用的方法。H2CrO4中Cr元素的化合价为__,其在水中的电离方程式为___。
(2)“酸浸”不能采用高温的原因是__,“滤液1”的主要溶质是__(写化学式)。
(3)相对于水洗,用浓HNO3洗涤的优点是__。
(4)“滤液2”中过量的H2CrO4被N2H4还原为Cr3+,同时放出无污染的气体,写出发生反应的离子方程式__。
(5)已知Cr(OH)3类似氢氧化铝,还原后溶液的pH不能大于8的原因是(用离子方程式说明理由)__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料、无机非金属材料、有机高分子材料是人类使用的三大类基础材料,它们以各自的特点满足着人类多方面的需要。
(1)金属材料中,有一类贮氢合金能够结合氢气形成金属化合物,并在一定条件下分解释放出氢气,该贮运原理属于_______变化,钢铁是制造轮船的主要金属材料,船身外通常装上一定数目比铁更活泼的金属块以防止腐蚀,该金属块可以选择_______(选填“铜块”、“锌块”、“铅块”);
(2)无机非金属材料中,用于电子工业的高纯碳酸钙、高纯氧化钙生产流程如下:

请回答下列问题:
①硝酸钙与碳酸铵在溶液中反应,其基本反应类型为_______;
②实验室常采用_______操作进行沉淀分离;
③生产高纯碳酸钙时,选择“220℃恒温干燥”而不选择“灼烧”的原因是_______;
④高纯氧化钙生产过程中,“干燥”的主要目的是为了防止______(用化学方程式表示);
(3)有机高分子材料“玉米塑料”,因其可降解被广泛用来替代一次性泡沫塑料,“玉米塑料”的使用可减少_______污染,20世纪30年代,尼龙因其抽成细丝极像蚕丝而被推向世界,生活中可采用______方法区分尼龙和蚕丝。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予锂离子电池的发明者,锂离子电池是目前应用广泛的一类电池。以钛铁矿(主要成分为FeTiO3,含有少量MgO、Fe2O3、SiO2等杂质)为原料,制备锂离子电池电极材料的工艺流程如图所示:
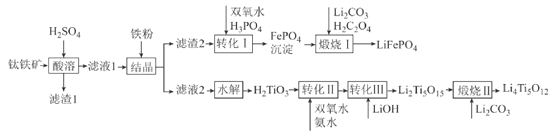
已知:①滤液1中含Ti微粒的主要存在形式为TiO2+;
②)Ksp(FePO4)=1.3×10-22、Ksp[Mg3(PO4)2]=1.0×10-24;溶液中某离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全。
请回答下列问题:
(1)滤渣1中主要成分的化学式为__。
(2)“结晶”温度需控制在70℃左右,若温度过高会导致的后果为__。
(3)“转化I”后所得溶液中c(Mg2+)=0.01mol·L-1,若其中Fe3+沉淀完全,则溶液中c(PO43-)的范围为__。
(4)“煅烧I”反应中氧化剂和还原剂的物质的量之比为__。
(5)“转化II”中H2TiO3的转化率(α)与温度(T)的关系如图所示。T0℃时,一定时间内H2TiO3的转化率最高的原因为__。
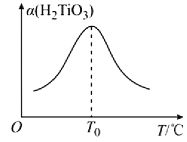
(6)Li2Ti5O15中-1价与-2价O原子的数目之比为___。“煅烧II”反应中同时生成两种参与大气循环的气体,该反应的化学方程式为__。
(7)某锂离子电池放电时的电池反应为Li1-xFePO4+LixC6=LiFePO4+6C,则充电时阳极的电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1的AgNO3溶液分别滴定体积均为50.0mL的由Cl-与Br-组成的混合溶液和由C1-与I-组成的混合溶液(两混合溶液中Cl-浓度相同,Br-与I-的浓度也相同),其滴定曲线如图所示。已知25℃时:Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=4.9×10-13,Ksp(AgI)=8.5×10-16。
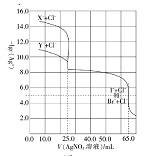
下列有关描述正确的是( )
A.图中X-为Br-
B.混合溶液中n(Cl-):n(I-)=8:5
C.滴定过程中首先沉淀的是AgCl
D.当滴入AgNO3溶液25mL时,Cl-与Br-组成的混合溶液中c(Ag+)=7×10-7mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二草酸合铜( II )酸钾晶体{K2[Cu(C2O4)2]·2H2O},微溶于冷水,可溶于热水,微溶于酒精,干燥时较为稳定,加热时易分解。
I.用氧化铜和草酸为原料制备二草酸合铜(II)酸钾晶体的流程如下:
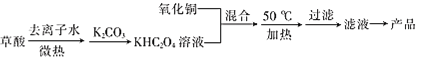
已知:H2C2O4![]() CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
回答下列问题:
(1)将H2C2O4晶体加入去离子水中,微热,溶解过程中温度不能太高,原因是________。
(2)将CuO与KHC2O4的混合液在50°C下充分反应,该反应的化学方程式为__________。
(3)50 °C时,加热至反应充分后的操作是_______________(填字母)。
A.放于冰水中冷却后过滤 B.自然冷却后过滤
C.趁热过滤 D.蒸发浓缩、冷却后过滤
II.以CuSO4·5H2O晶体和K2C2O4固体为原料制备二草酸合铜( II )酸钾晶体。
实验步骤:将CuSO4·5H2O晶体和K2C2O4固体分别用去离子水溶解后,将K2C2O4溶液逐滴加入硫酸铜溶液中,有晶体析出后放在冰水中冷却,过滤,用酒精洗涤,在水浴锅上炒干。炒时不断搅拌,得到产品。
(4)用酒精而不用冷水洗涤的目的是____________。
II.产品纯度的测定:准确称取制得的晶体试样ag溶于NH3·H2O中,并加水定容至250mL,取试样溶液25.00mL,再加入10 mL的稀硫酸,用b mol·L-1 的KMnO4标准液滴定,消耗KMnO4标准液V mL。
(5)滴定时,下列滴定方式中,最合理的是______(填字母),理由为________。 (夹持部分略去)
A. 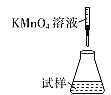 B.
B. 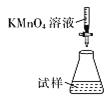 C.
C. 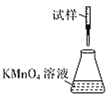
(6)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,实验结果会_____(填“偏大”偏小”或“无影响”)。
(7)该产品的纯度为___________(写出表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g) ![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积增大
A. ①②B. ①③C. ②③D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com