
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 0.2mol的铁与足量的稀硝酸反应,生成气体的分子效目为0.3NA
B. 常温常压下,14g由C2H4、C3H6组成的混合气体中含有碳原子的数目为NA
C. 2.24LCO2与足量的Na2O2反应.转移的电子总数必为0.1NA
D. 1L1mol/L的KAl(SO4)2溶液中阳离子总数为2NA
科目:高中化学 来源: 题型:
【题目】工业上制备水煤气的化学方程式如下:C(s)+H2O(g)![]() CO(g)+H2(g), 己知lmol的C完全反应吸收QkJ的热量,下列叙述正确的是
CO(g)+H2(g), 己知lmol的C完全反应吸收QkJ的热量,下列叙述正确的是
A. 增加C的量可以加快反应速率
B. 若将2molC 和足量的水蒸气混合,总共吸收的热量可为2QkJ
C. 反应至4 min时到平衡,若生成0.12mol H2,则CO的反应速率为0.03 mol/(L·min )
D. 当反应吸收热量为5QkJ时,断裂10NAH-O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24L丁烷中C—C键数目为0.4NA
B. 0.1mol葡萄糖分子中官能团数目为0.6NA
C. 28g N2和NO组成的混合物中分子数目可能为0.9NA
D. 1L pH =13的NaOH溶液中,Na+数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既可以鉴别乙烷和乙炔,又可以除去乙烷中含有的乙炔的方法是 ( )
A. 足量的溴的四氯化碳溶液 B. 与足量的液溴反应
C. 点燃 D. 在一定条件下与氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW,该温度下,将浓度为amol·L-1的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A. a=b
B. 混合溶液的pH=7
C. 混合溶液中c(H+)=![]() molL-1
molL-1
D. 混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g)
M(g)+N(g)
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.20 | a |
④ | 800 | 0.10 | 0.10 | b |
下列说法正确的是 ( )
A.实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率υ(N)=1.0×10-2mol/(L·min)
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为50%
D.实验④中,达到平衡时,b<0.05
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞中元素和化合物的说法,正确的是
A. 磷脂是细胞膜和各种细胞器的重要组成成分
B. ATP是由一分子腺苷、一分子核糖和三分子磷酸组成
C. DNA多样性与碱基数目、种类、排列顺序有关而与空间结构无关
D. 微量元素可参与某些复杂化合物的组成,如Fe、Mg分别参与血红蛋白和叶绿素组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下:Ksp(AgCl)=1.6×10-10,下列叙述正确的是 ( )
A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的小
B.AgCl的悬浊液中c(Cl-)=4×10-5.5mol/L
C.将0.001 mol·L-1AgNO3溶液滴入0.001 mol·L-1的KCl,无沉淀析出
D.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明Ksp(AgCl)<Ksp(AgBr)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.100mol·L-1的NaOH溶液分别滴定10.00mL 浓度均为0.100mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液电导率如图所示。下列说法不正确的是( )
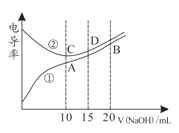
A.曲线①代表滴定CH3COOH溶液的曲线
B.在相同温度下,A、B、C 三点溶液中水电离的 c(H+):B<A=C
C.D点溶液中:c(Cl-)=2c(OH-)-2c(H+)
D.A点溶液中:c(CH3COO-)+c(OH-)-c(H+) = 0.05mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com