
【题目】25℃下列四种溶液:①c(H+)=1mol·L-1的醋酸②0.1mol·L-1的盐酸③0.01mol·L-1的NaOH溶液④c(OH-)=10-3mol·L-1氨水溶液。由水电离出的氢离子浓度之比为( )
A. 14∶13∶2∶3 B. 0∶1∶12∶11 C. 14∶13∶12∶11 D. 1∶10∶100∶1000
【答案】D
【解析】
水的电离平衡为H2O![]() H++OH-,在水中加入酸或者碱溶液,导致溶液中氢离子或者氢氧根离子浓度增大,抑制了水的电离;酸溶液中氢氧根离子是水电离的,碱溶液中氢离子是水电离,结合Kw=c(H+)×c(OH-)计算。
H++OH-,在水中加入酸或者碱溶液,导致溶液中氢离子或者氢氧根离子浓度增大,抑制了水的电离;酸溶液中氢氧根离子是水电离的,碱溶液中氢离子是水电离,结合Kw=c(H+)×c(OH-)计算。
酸溶液中,氢氧根离子是水电离的,碱溶液中氢离子是水电离的。
c(H+)=1mol·L-1的醋酸,溶液中c(H+)=1mol/L,c(H+)(水)=c(OH-)(水)=1×10-14mol/L;
0.1mol/L盐酸,溶液中c(H+)=0.1mol/L,c(H+)(水)=c(OH-)(水)=1×10-13mol/L;
0.01mol/L的NaOH 溶液,溶液中c(H+)=0.01mol/L,c(H+)(水)=c(OH-)(水)=1×10-12mol/L;
c(OH-)=10-3mol·L-1氨水溶液,溶液中c(OH-)=10-3mol·L-1,c(H+)(水)=c(OH-)(水)=1×10-11mol/L;
所以由水电离出的氢离子浓度之比为①:②:③:④=1×10-14mol/L:1×10-13mol/L:1×10-12mol/L:1×10-11mol/L=1:10:100:1000。
合理选项是D。


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】氮的化合物能影响植物的生长,其氧化物也是大气的主要污染物之一。
(1)固氮直接影响作物生长。自然固氮发生的反应有:
①N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ·mol-1
②2NO(g)+O2(g)==2NO2(g) ΔH2=-114.1kJ·mo1-l
③N2(g)+2O2(g)=2NO2(g) ΔH3=__________kJ ·mol-l。
(2)一定温度下,将等物质的量的NO和CO通入固定容积为4L的密闭容器中发生反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g),反应过程中CO的物质的量变化如图甲所示:
N2(g)+2CO2(g),反应过程中CO的物质的量变化如图甲所示:
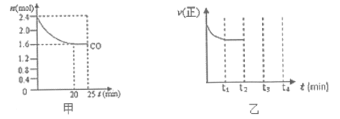
①能判断反应已达到化学平衡状态的是___________(填序号);
A.容器中的压强不变
B.2v正(CO)=v逆(N2)
C.气体的平均相对分子质量保持不变
D.NO和CO的体积比保持不变
②0~20min平均反应速率v(NO)为_______mol/(L·min);
③反应达平衡后再向容器中加入0.4molCO和0.4molCO2,则此时平衡______(填“向正反应方向移动”、“向逆反应方向移动”或“不移动”);
④该反应的正反应速率如图乙所示。在t2时刻,将容器的容积迅速扩大到原来的2倍,在其他条件不变的情况下,t3时刻达到新的平衡状态。请在上图乙中,补充画出从t2到t4时刻正反应速率随时间的变化曲线。_____________;
(3)三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2,其反应分两步进行。第一步是:C3N3(OH)3![]() 3HCNO;第二步是HCNO与NO2反应,把氮元素和碳元素转变成无毒气体。请写出第二步发生的化学反应方程式_________________;
3HCNO;第二步是HCNO与NO2反应,把氮元素和碳元素转变成无毒气体。请写出第二步发生的化学反应方程式_________________;
(4)常温下,在x mol·L-1氨水中加入等体积的y mol·L-1硫酸得混合溶液M恰好显中性。
①M溶液中所有离子浓度由大到小的顺序为_________________。
②常温下,NH3·H2O的电离常数K=_______________(用含x和y的代数式表示,忽略溶液混合前后的体积变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型NaBH4/H2O2燃料电池DBFC的结构如图所示,该电池总反应方程式:NaBH4 +4H2O2= NaBO2+ 6H2O,有关的说法不正确的是

A. 电极B为正极
B. 放电过程中,Na+从正极区向负极区迁移
C. 电池负极的电极反应为:BH4-+8OH8e=BO2-+6H2O
D. 在电池反应中,每消耗1L6mol/LH2O2溶液,理论上流过电路中的电子为12NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
B.过氧化钠常用于呼吸面具和潜水艇里氧气的供给
C.a g H2与氧气充分燃烧后的产物被Na2O2完全吸收,Na2O2固体增重a g
D.2.3g金属钠与氧气完全反应生成Na2O和Na2O2的混合物,失去0.1mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是一种应用广泛的金属,在工业上用![]() 和冰晶石
和冰晶石![]() 混合熔电解制得。
混合熔电解制得。
Ⅰ.铝土矿的主要成分是![]() 和
和![]() 等。从铝土矿中提炼
等。从铝土矿中提炼![]() 的流程如下:
的流程如下:

(1)写出反应1中涉及的任意一个化学方程式______;
(2)滤液Ⅰ中加入的CaO生成的沉淀是_____,已知气体A在标准状况下的密度为1.96g/L,反应2的离子方程式为______;
Ⅱ.以萤石![]() 和纯碱为原料制备冰晶石的流程如下:
和纯碱为原料制备冰晶石的流程如下:

(3)萤石![]() 的电子式______;
的电子式______;
(4)若E为硫酸钙,D为最稳定的气态氢化物,则化合物C是______,写出由D制备冰晶石![]() 的化学方程式_______;
的化学方程式_______;
(5)工业电解制铝若以石墨为电极,阳极产生的混合气体的成分是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是
A. 向0.1 mol·L1 Na2CO3溶液中通入适量CO2气体后:c(Na+)=2[c(![]() )+c(
)+c(![]() )+c(H2CO3)]
)+c(H2CO3)]
B. 常温下,pH=6的NaHSO3溶液中:c(![]() )c(H2SO3)=9.9×107 mol·L1
)c(H2SO3)=9.9×107 mol·L1
C. 等物质的量浓度、等体积的Na2CO3和NaHCO3混合:![]() <
<![]()
D. 0.1 mol·L1 Na2C2O4溶液与0.1 mol·L1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(![]() )+c(
)+c(![]() )+c(OH)=c(Na+)+c(H+)
)+c(OH)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解
D. a和b用导线连接后,Fe片上发生还原反应,溶液中的Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:

常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀 | 7.5 | 2.7 | 4.8 |
完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)炉气中的有害气体成分是__________,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为__________。
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:__________。并写出H2O2的电子式__________,Fe(铁)在元素周期表中的位置:__________;当试剂X是__________时,更有利于降低生产成本。
(3)加入试剂Y调pH时,pH的调控范围是__________。
(4)操作X包括__________、洗涤、烘干,其中烘干时要隔绝空气,其目的是__________。
(5)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素在周期表中的位置如图所示,其中R元素原子的最外层电子数等于其电子层数的2倍,下列判断正确的是

A. 元素的非金属性次序为:Y>X>M
B. 气态氢化物稳定性:M>R
C. Z的氧化物可以做光导纤维
D. 最D高价氧化物对应水化物的酸性:Y>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com