
ΓΨΧβΡΩΓΩ“―÷Σ–ΩΗζ≈®ΝρΥαΖ¥”Π…ζ≥…SO2Θ§ΗζœΓΝρΥαΖ¥”Π…ζ≥…H2ΓΘ Ι“ΜΕ®ΝΩΒΡ–Ω”κ100mL18.5molΓΛLΘ≠1≈®ΝρΥα≥δΖ÷Ζ¥”ΠΘ§–ΩΆξ»Ϊ»ήΫβΘ§Ά§ ± ’Φ·ΒΫ±ξΉΦΉ¥Ωωœ¬ΒΡΤχΧεA33.6LΓΘΫΪΖ¥”ΠΚσΒΡ»ή“ΚœΓ ΆΒΫ1LΘ§≤βΒΟ»ή“Κ÷–«βάκΉ”ΒΡ≈®Ε»ΈΣ0.1molΓΛLΘ≠1ΓΘ
Θ®1Θ©–¥≥ω–ΩΗζ≈®ΝρΥαΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ____ΓΘ
Θ®2Θ©Ζ¥”ΠΙΐ≥Χ÷–œϊΚΡΒΡH2SO4ΒΡΈο÷ ΒΡΝΩ «____ΓΘ
Θ®3Θ©ΤχΧεAΒΡ≥…Ζ÷ «____Θ§Ης≥…Ζ÷ΒΡΧεΜΐ±» «____ΓΘ
Θ®4Θ©Ζ¥”ΠΙΐ≥Χ÷–œϊΚΡΒΡ–ΩΒΡ÷ ΝΩ «____ΓΘ
ΓΨ¥πΑΗΓΩZnΘΪ2H2SO4(≈®)=ZnSO4ΘΪSO2ΓϋΘΪ2H2O 1.80mol Εΰ―θΜ·ΝρΚΆ«βΤχ 1ΓΟ4 97.5g
ΓΨΫβΈωΓΩ
Δ≈–ΩΗζ≈®ΝρΥαΖ¥”Π…ζ≥…ΝρΥα–ΩΓΔΕΰ―θΜ·ΝρΚΆΥ°ΓΘ
ΔΤΖ¥”ΠΙΐ≥Χ÷–œϊΚΡH2SO4ΒΡΈο÷ ΒΡΝΩΒ»”ΎΉήΒΡΝρΥαΦθ»Ξ Θ”ύΒΡΝρΥαΓΘ
Δ«œ»ΥψΤχΧεAΒΡΈο÷ ΒΡΝΩΘ§‘ΌΗυΨίΧβ“β”ΟΦΪœόΥΦΈ§≈–Εœ «ΖώΈΣΒΞ“ΜΤχΧεΘ§ΗυΨίΕΰ―θΜ·ΝρΚΆ«βΤχΈο÷ ΒΡΝΩΚΆ ΊΚψΙΊœΒΫ®ΝΔΙΊœΒ ΫΦΤΥψΓΘ
Δ»ΗυΨίΝΫΗωΜ·―ßΖΫ≥Χ ΫΩ…÷Σn(Zn)ΘΫn(SO2)ΘΪn(H2)ΦΤΥψΓΘ
Δ≈–ΩΗζ≈®ΝρΥαΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚZnΘΪ2H2SO4(≈®)=ZnSO4ΘΪSO2ΓϋΘΪ2H2OΓΘ
ΔΤΖ¥”ΠΙΐ≥Χ÷–œϊΚΡH2SO4ΒΡΈο÷ ΒΡΝΩΈΣ![]() Θ§Ι ¥πΑΗΈΣΘΚ1.8molΓΘ
Θ§Ι ¥πΑΗΈΣΘΚ1.8molΓΘ
Δ«ΤχΧεAΒΡΈο÷ ΒΡΝΩ![]()
ΗυΨίΧβ“βΘ§–ΩΗζΝρΥαΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «ΘΚ
ZnΘΪ2H2SO4(≈®)ΘΫZnSO4ΘΪSO2ΓϋΘΪ2H2OΔΌ
ZnΘΪH2SO4(œΓ)ΘΫZnSO4ΘΪH2ΓϋΔΎ
»τ…ζ≥…ΒΡΤχΧε»Ϊ «Εΰ―θΜ·ΝρΘ§‘ρœϊΚΡH2SO4ΒΡΈο÷ ΒΡΝΩΈΣn(H2SO4)ΘΫ2ΓΝn(SO2)ΘΫ2ΓΝ1.5 molΘΫ3.0 molΓΌ1.8 molΘ§Υυ“‘¥ΥΦΌ…η≤Μ≥…ΝΔΘ§Φ¥ΗΟΤχΧε÷ΜΡή «Εΰ―θΜ·ΝρΚΆ«βΤχΒΡΜλΚœΤχΧεΓΘ
…ηΗΟΜλΚœΤχΧε÷–Εΰ―θΜ·ΝρΚΆ«βΤχΒΡΈο÷ ΒΡΝΩΖ÷±π «xΚΆyΓΘΗυΨίΧβ“βΩ…ΒΟ»γœ¬ΝΫΗωΖΫ≥ΧΘΚ
xΘΪyΘΫ1.5 molΘ§2xΘΪyΘΫ1.8 molΓΘ
ΝΣΝΔΘ§ΫβΒΟxΘΫ0.3 molΘ§yΘΫ1.2 molΘ§![]() Θ§Ι ¥πΑΗΈΣΘΚΕΰ―θΜ·ΝρΚΆ«βΤχΘΜ1ΓΟ4ΓΘ
Θ§Ι ¥πΑΗΈΣΘΚΕΰ―θΜ·ΝρΚΆ«βΤχΘΜ1ΓΟ4ΓΘ
Δ»ΗυΨίΝΫΗωΜ·―ßΖΫ≥Χ ΫΩ…÷Σn(Zn)ΘΫn(SO2)ΘΪn(H2)ΘΫ1.5 molΘ§‘ρm(Zn)ΘΫ65 gΓΛmolΘ≠1ΓΝ1.5 molΘΫ97.5 gΘ§Ι ¥πΑΗΈΣΘΚ97.5gΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΥυœ¬Ν–Μ·―ß”Ο”οΒΡάμΫβ’ΐ»ΖΒΡ «Θ® Θ©
A.±»άΐΡΘ–Ά![]() Φ»Ω…“‘±μ ΨΦΉΆιΖ÷Ή”Θ§“≤Ω…“‘±μ ΨΥΡ¬»Μ·ΧΦΖ÷Ή”
Φ»Ω…“‘±μ ΨΦΉΆιΖ÷Ή”Θ§“≤Ω…“‘±μ ΨΥΡ¬»Μ·ΧΦΖ÷Ή”
B.ΒγΉ” Ϋ![]() HΦ»Ω…“‘±μ Ψτ«ΜυΘ§“≤Ω…“‘±μ Ψ«β―θΗυάκΉ”
HΦ»Ω…“‘±μ Ψτ«ΜυΘ§“≤Ω…“‘±μ Ψ«β―θΗυάκΉ”
C.±ϊœ©ΒΡΉνΦρ ΫΩ…±μ ΨΈΣCH2
D.ΫαΙΙΦρ Ϋ(CH3)2CHCH3Φ»Ω…“‘±μ Ψ’ΐΕΓΆιΘ§“≤Ω…“‘±μ Ψ“λΕΓΆι
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩNaCl»ή“Κ÷–Μλ”–Na2SO4ΓΔCaCl2»ή“ΚΚΆΒμΖέΫΚΧεΘ§―Γ‘ώ Β±ΒΡ ‘ΦΝΚΆΖΫΖ®¥”÷–Χα¥Ω≥ωNaClΨßΧεΓΘœύ”ΠΒΡ Β―ιΙΐ≥Χ»γΆΦΘΚ
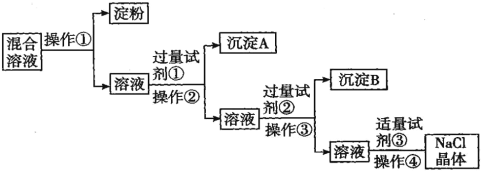
(1)≤ΌΉςΔΌΒΡΟϊ≥Τ «___________
(2) ‘ΦΝΔΌΒΡΜ·―ß Ϋ «____________ ≈–Εœ ‘ΦΝΔΌ“―ΙΐΝΩΒΡΖΫΖ® «ΘΚ________________________
(3)Φ”»κ ‘ΦΝΔΎΖΔ…ζΒΡάκΉ”ΖΫ≥Χ Ϋ «____________________________________ΓΘ
(4)≤ΌΉςΔήΒΡΟϊ≥Τ «ΘΚ_____________
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Έο÷ “ΜΕ® τ”ΎΆ§œΒΈοΒΡ «Θ® Θ©
ΔΌ![]() ΔΎ
ΔΎ![]() Δέ
Δέ![]() ΔήC2H4 ΔίCH2=CHΓΣCH=CH2 ΔόC3H6 ΔΏ
ΔήC2H4 ΔίCH2=CHΓΣCH=CH2 ΔόC3H6 ΔΏ![]() Δύ
Δύ![]()
A.ΔήΚΆΔόB.ΔΌΓΔΔΎΚΆΔέC.ΔήΓΔΔόΚΆΔύD.ΔίΚΆΔΏ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΛ“Β…œ≥ΘΆ®ΙΐΗΏΈ¬Ζ÷ΫβFeSO4ΒΡΖΫΖ®÷Τ±ΗFe2O3Θ§ΤδΜ·―ßΖΫ≥Χ ΫΈΣΘΚ2FeSO4![]() Fe2O3ΘΪSO2ΓϋΘΪSO3ΓϋΓΘΈΣΦλ―ιFeSO4ΗΏΈ¬Ζ÷ΫβΒΡ≤ζΈοΘ§Ϋχ––»γœ¬ Β―ιΘΚ
Fe2O3ΘΪSO2ΓϋΘΪSO3ΓϋΓΘΈΣΦλ―ιFeSO4ΗΏΈ¬Ζ÷ΫβΒΡ≤ζΈοΘ§Ϋχ––»γœ¬ Β―ιΘΚ
ΔΌ»Γ…ΌΝΩFeSO4ΗΏΈ¬Ζ÷ΫβΒΟΒΫΒΡΙΧΧεΘ§Φ”“ΜΕ®ΝΩœΓ―ΈΥα»ήΫβΘ§œρΗΟ»ή“Κ÷–Φ”»κ ΝΩΒΡKSCN»ή“ΚΘ§Ιέ≤λ»ή“Κ―’…ΪΒΡ±δΜ·“‘Φλ―ιFe3ΘΪ «Ζώ¥φ‘ΎΓΘ
ΔΎΫΪFeSO4ΗΏΈ¬Ζ÷Ϋβ≤ζ…ζΒΡΤχΧεΆ®»κ»γΆΦΥυ ΨΒΡΉΑ÷Ο÷–Θ§“‘Φλ―ι≤ζ…ζΒΡΤχΧε÷– «ΖώΚ§”–SO2ΓΔSO3ΓΘ
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
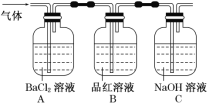
Θ®1Θ©–¥≥ωKSCN»ή“Κ”κFe3ΘΪΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚ____ΓΘ
Θ®2Θ©≤ΌΉςΔΎ÷–Ιέ≤λΒΫΒΡœ÷œσΚΆΫα¬έ «____ΘΜ_____ΓΘ
Θ®3Θ©≤ΌΉςΔΎ÷–ΉνΚσ“ΣΫΪΆ®ΙΐΤΖΚλ»ή“ΚΒΡΤχΧεΆ®»κNaOH»ή“Κ÷–ΒΡ‘≠“ρ «___Θ§”–ΙΊΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ____ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕΧ÷ήΤΎ÷ςΉε‘ΣΥΊXΓΔYΓΔZΓΔW‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§AΓΔBΓΔCΓΔDΓΔEΈΣΤδ÷–ΝΫ÷÷‘ΣΥΊΉι≥…ΒΡ≥ΘΦϊΜ·ΚœΈοΘ§ΜυΧ§Z‘≠Ή”ΚΥΆβ”–ΝΫΗωΈ¥≥…Ε‘ΒγΉ”Θ§AΓΔDΨυΚ§”–10ΗωΒγΉ”«“÷––Ρ‘≠Ή”ΒΡ‘”Μ·ΖΫ ΫœύΆ§Θ§ΥϋΟ«÷°ΦδΒΡΉΣΜ·ΙΊœΒ»γΆΦΥυ Ψ(≤ΩΖ÷Ζ¥”ΠΈοΜρ…ζ≥…Έο Γ¬‘)Θ§œ¬Ν–ΥΒΖ®÷–≤Μ’ΐ»ΖΒΡ «Θ® Θ©
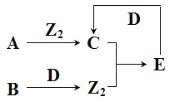
A.ΦρΒΞάκΉ”ΑκΨΕΘΚY>Z>W
B.»τC÷–Μλ”–EΩ…”ΟΥ°œ¥ΖΫΖ®≥ΐ»Ξ
C.ΟΩΗωDΖ÷Ή”÷ήΈßΩ…“‘–Έ≥…4Ηω«βΦϋ
D.B”κDΖ¥”Π…ζ≥…Z2 ±Θ§DΉςΜΙ‘≠ΦΝ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ2017ΡξΘ§÷–ΆβΩΤ―ßΦ“Ά≈Ε”Ι≤Ά§Κœ≥…T-ΧΦΓΘT-ΧΦΒΡΫαΙΙ «ΫΪΝΔΖΫΫπΗ’ ·÷–ΒΡΟΩΗωΧΦ‘≠Ή””Ο“ΜΗω”…4ΗωΧΦ‘≠Ή”Ήι≥…ΒΡ’ΐΥΡΟφΧεΫαΙΙΒΞ‘Σ»Γ¥ζ–Έ≥…ΧΦΒΡ“Μ÷÷–¬–Ά»ΐΈ§ΝΔΖΫΨßΧεΫαΙΙΘ§»γΆΦΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ®ΓΓ ΓΓΘ©

A.ΟΩΗωT-ΧΦΨßΑϊ÷–Κ§32ΗωΧΦ‘≠Ή”
B.T-ΧΦ÷–ΧΦ”κΧΦΒΡΉν–ΓΦ–Ϋ«ΈΣ109.5ΓΘ
C.T-ΧΦ τ”Ύ‘≠Ή”ΨßΧε
D.»γΆΦ «T-ΧΦΨßΑϊΒΡΗ© ”ΆΦ

≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ΘΈ¬œ¬Θ§100mL0.1molΓΛL-1ΒΡH2A»ή“Κ÷–ΒΈΦ”0.1molΓΛL-1NaOH»ή“ΚΘ§Κ§A‘ΣΥΊœύΙΊΈΔΝΘΈο÷ ΒΡΝΩΥφpHΒΡ±δΜ·»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
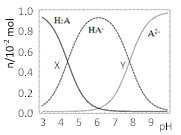
A.ΫΪΒ»≈®Ε»Β»ΧεΜΐΒΡNa2A”κH2A»ή“ΚΜλΚœΚσΘ§»ή“Κœ‘Φν–‘
B.XΒψΥυΦ”NaOH»ή“ΚΧεΜΐΈΣ50mL
C.XΒψ»ή“Κ÷–Κ§A‘ΣΥΊΒΡœύΙΊάκΉ”¥φ‘Ύ“‘œ¬ΙΊœΒΘΚc(H2A)+c(HA-)+c(A2-)=0.1molΓΛL-1
D.YΒψ»ή“Κ÷–¥φ‘Ύ“‘œ¬ΙΊœΒΘΚc(H+)+c(Na+)=c(OH-)+3c(HA-)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕΧ÷ήΤΎ‘ΣΥΊXΓΔYΩ…“‘–Έ≥…Μ·ΚœΈο![]() Θ§Β±XΒΡ‘≠Ή”–ρ ΐΈΣmΘ§YΒΡ‘≠Ή”–ρ ΐΩ…Ρή «
Θ§Β±XΒΡ‘≠Ή”–ρ ΐΈΣmΘ§YΒΡ‘≠Ή”–ρ ΐΩ…Ρή «![]()
ΔΌm-8 ΔΎm+4 Δέm+2 Δήm+10 Δίm-6 Δόm+1 ΔΏm+9 Δύm+5
A.ΔΌΔΎΔέB.ΔΌΔέΔήΔίΔόΔύ
C.ΔΌΔέΔίΔόΔύD.ΔΌΔΎΔέΔήΔίΔόΔΏ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com