
【题目】下列过程需要吸收能量的是
A.碘的升华B.酒精燃烧C.酸碱中和D.2H→H2
科目:高中化学 来源: 题型:
【题目】以下反应会导致溶液导电性减弱最明显的是( )
A.Na2SO4溶液加入BaCl2固体
B.Ba(OH)2溶液中加入CuSO4(少量)固体
C.NaOH溶液通入HCl
D.H2O中加入NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是_________,CO的体积分数是_________,混合气体的平均摩尔质量是____________。
(2) 1.15g金属钠跟水反应,得到100mL溶液,试计算:
①生成的气体在标准状况下是_________________
②反应后所得溶液的物质的量浓度是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学需要借助化学专用语言来描述,下列有关化学用语不正确的是( )
A. 钠离子的电子式:Na+ B. Cl—的结构示意图:![]()
C. 氖气的化学式:Ne D. 质量数为18的氧原子:818O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图的锥形瓶内充满干燥气体X,滴管内盛有液体Y,将滴管内的液体挤压到锥形瓶中,轻轻振荡,一会儿可见小气球a鼓涨,下列X和Y的组合不可能的是( )
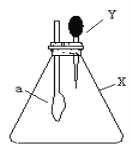
X | Y | |
A | HCl | 饱和食盐水 |
B | H2 | 浓硫酸 |
C | HCl | 2mol/L NaOH溶液 |
D | Cl2 | 6mol/L NaOH 溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物在工农业生产中都有重要应用。
(1)氨和肼(N2H4)是两种最常见的氮氢化物。
己知:4NH3(g)+3O2(g) ![]() 2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g)
2N2(g)+6H2O(g) ΔH1=-541.8kJ/mol,化学平衡常数为K1。N2H4(g)+O2(g) ![]() N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为_________,该反应的化学平衡常数K=____(用K1、K2表示)。
N2(g)+2H2O(g) ΔH2=-534kJ/mol,化学平衡常数为K2。则用NH3和O2制取N2H4的热化学方程式为_________,该反应的化学平衡常数K=____(用K1、K2表示)。
(2)对于2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
①下列能说明该反应已经达到平衡状态的是____(填字母代号)。
A.c(CO)=c(CO2) B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆 D.容器中混合气体的平均摩尔质量不变
②图1为容器内的压强(P)与起始压强(P0)的比值(P/P0)随时间(t)的变化曲线。0~5min内,该反应的平均反应速率v(N2)= ____,平衡时NO的转化率为____。
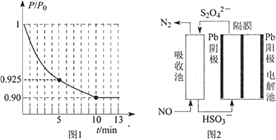
(3)使用间接电化学法可处理燃煤烟气中的NO,装置如图2所示。已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式_________。用离子方程式表示吸收池中除去NO的原理__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是“聚宝盆”,工业上,人们直接从海水中得到食盐。海水在浓缩过程中析出盐类物质的种类和质量,如下表:
海水密度(g/L) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
1.13 | 0.56 | ||||
1.20 | 0.91 | ||||
1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
(1)常采用____________的方法从海水中得到食盐。
(2)为得到含杂质较少的食盐,实际生产中卤水的密度控制在_____之间。
(3)粗盐中常含有MgCl2、MgSO4、CaCl2等杂质,通常在实验室中依次加入_________、__________、___________、___________等四种物质除去杂质。(填化学式)
(4)电解饱和食盐水可以制取氯气,同时得到几种重要的化工产品,
该反应的化学方程式为_________________________________________。通电时阳极产物是__________该产物的检验方法是___________________________________________
(5)电解过程中得到气体物质还可以化合为HCl,在实验室中我们利用_________________和_____________ 反应(写名称)来制取。该气体__________________溶于水,可以做喷泉实验。写出氯化氢气体溶于水后的电离方程式_____________________________________
(6)新制的氯水显_______色,这是因为氯水中有__________(填微粒符号)存在。向氯水中滴入几滴AgNO3溶液,观察到的现象是____________________________,发生变化的化学方程式为______________________________________________。蓝色石蕊试纸遇到氯水后的现象是___________________________,氯气有毒,不能直接排放到空气中,需要用________________________来吸收,写出反应的化学方程式为_________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离或提纯物质的方法正确的是( )
A.用蒸馏的方法制取蒸馏水
B.用过滤的方法除去NaCl溶液中含有的少量淀粉胶体
C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D.用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜矿石又叫孔雀石。已知碱式碳酸铜粉末不溶于水和醇,用CuSO4溶液与Na2CO3溶液反应可以得到碱式碳酸铜,为了探究该反应得到的碱式碳酸铜的化学式,某班同学设计了如下实验:
【碱式碳酸铜的制备】
称取12.5g胆矾,研细,滴加4滴稀硫酸,溶于适量蒸馏水中,充分搅拌后得到CuSO4溶液。向其中加入适量Na2CO3溶液,充分振荡,将所得蓝绿色悬浊液静置后过滤,依次用蒸馏水、无水乙醇洗涤所得蓝绿色固体,最后低温烘干备用。
(1)配制CuSO4溶液时,滴加稀硫酸的作用是__________________________________。
(2)用无水乙醇洗涤蓝绿色固体的目的是_____________________________________。
【实验探究】
同学们设计了如下装置,用制得的蓝绿色固体进行实验。
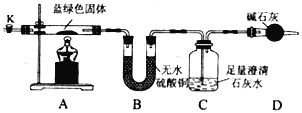
请按要求答下列问题:
(3)检查完该装置的气密性,装入药品后,实验开始前需通入一段时间气体N2,然后关闭弹簧夹K,再点燃A处酒精灯加热,控制C中导管均匀地产生气泡。通入N2的作用是____________,N2的电子式为____________。
(4)点燃A处酒精灯后,能观察到的现象是_________________________________。
(5)装置C中所发生反应的离子方程式为_____________________________________。
(6)同学们查阅文献得知:Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,经讨论认为用Ba(OH)2代替Ca(OH)2来定量测定蓝绿色固体的化学式会更好,其原因是_________________(选填下列字母代号)。
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收 CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
(7)若蓝绿色固体的组成为xCuCO3·yCu(OH)2。取干燥后的蓝绿色固体10.84g,煅烧至完全分解后得到8.00g固体及1.08gH2O。则该蓝绿色固体的化学式为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com