
【题目】(1)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g。此混合物中CO和CO2的物质的量之比是_________,CO的体积分数是_________,混合气体的平均摩尔质量是____________。
(2) 1.15g金属钠跟水反应,得到100mL溶液,试计算:
①生成的气体在标准状况下是_________________
②反应后所得溶液的物质的量浓度是______________________
【答案】1:3 25% 40g/mol 0.56L或560ml 0.5mol/L
【解析】
以物质的量为中心,列方程组解混合物的计算问题、列比例解化学方程式的计算问题。
(1)设混合气体中CO、CO2的物质的量分别是x、y,则(x+y)×22.4L/mol=8.96L,28g/mol×x+44g/mol×y=16g。解方程组得x=0.1mol,y=0.3mol。
故混合气体中,CO和CO2的物质的量之比是0.1mol:0.3mol=1:3,CO的体积分数是![]() =25%,混合气体的平均摩尔质量
=25%,混合气体的平均摩尔质量![]() =40g/mol。
=40g/mol。
2Na + 2H2O = 2NaOH + H2↑
46g 2mol 22.4L
1.15g n(NaOH) V(H2)
①生成的氢气在标准状况时体积V(H2)=0.56L;
②反应生成n(NaOH)=0.05mol,则溶液的物质的量浓度c(NaOH)=0.5mol/L。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】某课外兴趣小组需要用 18 mol/L 的浓硫酸配制80mL 3.0 mol/L 稀硫酸的实验步骤如下: ① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 稀释 ④ 检漏、 转移、洗涤⑤ 定容、摇匀 回答下列问题:
(1)所需浓硫酸的体积是__________ mL, 量取浓硫酸所用的量筒的规格是___________ (用下列编号填空) 。
A.10 mL B.25 mL C.50 mL D.100 mL
(2)第⑤步实验的操作是继续向容量瓶中注入蒸馏水至离刻度线__________, 改用___________向容量瓶中滴加蒸馏水至_________________________为止。塞紧瓶塞,倒转摇匀并转移至试剂瓶中。
(3)下列情况对所配制的稀硫酸浓度有何影响? (填 “ 偏大 ”“ 偏小 ” 或 “ 无影响”)
①容量瓶用蒸馏水洗涤后残留有少量的水_________________
②在转入容量瓶前烧杯中溶液未冷却至室温_________
③取完浓硫酸后洗涤量筒,并把洗涤液倒入烧杯___________。
④定容结束时俯视刻度线_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝广泛应用于电子陶瓷等工业领域。在一定条件下,AlN可通过以下反应合成:Al2O3+N2+3C![]() 2AlN+3CO。有关该反应下列叙述正确的是
2AlN+3CO。有关该反应下列叙述正确的是
A. AlN中氮的化合价为-3 B. 上述反应中,每消耗1 mol N2需转移3 mol电子
C. AlN的摩尔质量为41 g D. 上述反应中,N2是还原剂,Al2O3是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用键能的大小来解释的是 ( )
A.N元素的电负性较大,但N2的化学性质很稳定
B.稀有气体一般难发生化学反应
C.HF、HCl、HBr、HI的稳定性逐渐减弱
D.F2比O2更容易与H2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是 ( )
A. 铜铸塑像上出现铜绿[Cu2(OH)2CO3] B. 充有氢气的气球遇明火爆炸
C. 大理石雕像被酸雨腐蚀毁坏 D. 铁质菜刀生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是
A. NaHCO3的水解:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. 醋酸的电离:CH3COOH=CH3COO-+H+
C. 碳酸钙的溶解平衡:CaCO3(s)![]() Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
D. H2的燃烧热为285.8 kJ/mol,则表示H2燃烧热的热化学方程式为:H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用还原铁粉处理含Fe(NO3)3、Cu(NO3)2、HNO3的废水,所加还原铁粉的质量与溶液中Fe2+的浓度变化关系如下图(忽略溶液体积变化)。下列有关结论错误的是( )
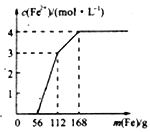
A. 加入铁粉质量小于56g时发生的反应为Fe+NO3-+4H+=Fe3++NO↑+2H2O
B. 当加入的铁粉质量超过168g后,溶液中的溶质只含有Fe(NO3)2(忽略Fe2+的水解)
C. 原废水中Fe(NO3)3的浓度为2mol/L,Cu(NO3)2的浓度均为1mol/L
D. 原废水中三种物质的氧化性由强到弱的顺序是HNO3>Fe(NO3)3>Cu(NO3)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com