
| ʵ�� ��� | �¶� | ��ʼpH | 0.1mol/L ������Һ/mL | 0.01mol/L KMnO4�ܵ� ���/mL | ����ˮ ���/mL | �������ݣ���Ӧ���Һ��ɫ ʱ��/s�� |
| �� | ���� | 1 | 20 | 50 | 30 | t1 |
| �� | ���� | 2 | 20 | 50 | 30 | t2 |
| �� | ���� | 2 | 40 | a | b | t3 |
| ʵ�鷽������Ҫ��д������������̣� | Ԥ��ʵ�����ͽ��� |
| ����Ӧ���Һ��ɫʱ��С��ʵ����е�t1����MnSO4�Ը÷�Ӧ������ã�����ɫʱ����ͬ����MnSO4�Ը÷�Ӧ�����ã� |
���� ��1��ʵ��Ҫ�����KMnO4��Һ��ʼŨ����ͬ�����������Ϊ100mL������ˮ�������
��2�������������ط�Ӧ�������ӺͶ�����̼��ˮ��
��3��ʵ��ٺ͢�ֻ��pH��ͬ��������������ͬ��
��4������������Ӧ������ʵ�����ͬ���������̽��жԱ�ʵ�飻
��5���ٲ��ᷴӦ��ϣ��������һ��KMnO4��Һ����Һ��Ϊ��ɫ����ɫ30s�ڲ���ȥ��˵���ζ����յ㣻
������������Ũ�ȣ����ɹ�ϵʽ2KMnO4��5H2C2O4���㣮
��� �⣺��1��ʵ��Ҫ�����KMnO4��Һ��ʼŨ����ͬ����KMnO4��Һ�����Ϊ50mL�������Ϊ100mL����ˮ�����10mL��
�ʴ�Ϊ��50��10��
��2�������������ط�Ӧ�������ӺͶ�����̼��ˮ���䷴Ӧ�����ӷ���ʽΪ��5H2C2O4+2MnO4-+6H+=10CO2��+2Mn2++8H2O��
�ʴ�Ϊ��5H2C2O4+2MnO4-+6H+=10CO2��+2Mn2++8H2O��
��3��ʵ��ٺ͢�ֻ��pH��ͬ��������������ͬ������t1��t2��˵����Һ��pH�Ը÷�Ӧ��������Ӱ�죬
�ʴ�Ϊ����Һ��pH�Ը÷�Ӧ��������Ӱ�죻
��4������������Ӧ������ʵ�����ͬ���������̽��жԱ�ʵ�飬����Ӧ���Һ��ɫʱ��С��ʵ����е�t1����MnSO4�Ը÷�Ӧ������ã�����ɫʱ����ͬ����MnSO4�Ը÷�Ӧ�����ã���
�ʴ�Ϊ��
| ʵ�鷽������Ҫ��д����������̣� | Ԥ��ʵ�����ͽ��� |
| ����Ӧ���Һ�м�������MnSO4���壬����������Ӧ������ʵ�����ͬ�����жԱ�ʵ�� | ����Ӧ���Һ��ɫʱ��С��ʵ����е�t1����MnSO4�Ը÷�Ӧ������ã�����ɫʱ����ͬ����MnSO4�Ը÷�Ӧ�����ã� |
���� ������Ҫ���ʵ�鿼����Ӱ�컯ѧ��Ӧ���ʵ����أ���Ŀ�Ѷ��еȣ�ע�������¶ȡ�Ũ�ȡ������Ի�ѧ��Ӧ���ʵ�Ӱ�죬���ö���������̽����������Է�Ӧ���ʵ�Ӱ��ʱ�����뱣֤����Ӱ�췴Ӧ���ʵ�����һ�£������ڿ���ѧ���ķ��������ͼ���������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ��pH�Ĵ�С˳���Ǣ٣��ڣ��� | |
| B�� | ������Һϡ����ͬ������pH�仯�����Ǣ� | |
| C�� | ������Һ�к����������˳���ǣ��ڣ��٣��� | |
| D�� | ������Һ����ˮ�����c��H+����С˳���ǣ��ۣ��ڣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ŀǰ��ֱ�����õ���Դ�����ɻ�ѧ��Ӧ������ | |
| B�� | ú��ʯ�ͣ���Ȼ���ǵ�����������Ҫ�����ֻ�ʯȼ�� | |
| C�� | ���������Դ��ú̿ | |
| D�� | �����˶������ĵ������뻯ѧ��Ӧ�й� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H��0��ʾ���ȷ�Ӧ����H��0��ʾ���ȷ�Ӧ | |
| B�� | 0.5 mol H2SO4��0.5 mol Ba��OH��2��ȫ��Ӧ����BaSO4ʱ�ų����Ƚ����к��� | |
| C�� | 1 mol H2��0.5 mol O2��Ӧ�ų����Ⱦ���H2��ȼ���� | |
| D�� | �Ȼ�ѧ����ʽ�еĻ�ѧ������ֻ��ʾ���ʵ����������Ƿ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ���� | ���� |
| A | ij��ɫ����ͨ�����ʯ��ˮ�� | ���ɰ�ɫ���� | ������һ����CO2 |
| B | ������ͭƬ����Ũ������ | ���������� | ������ͭ��Ũ����ۻ� |
| C | �ýྻ����˿պȡij��Һ������ɫ��Ӧʵ�� | ����ʻ�ɫ | ����Һ����Na+��һ������K+ |
| D | ��KI��FeCl3��Һ���Թ��л�Ϻ���CCl4�������� | �²���Һ���Ϻ�ɫ | �����ԣ�Fe3+��I2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N2�ĵ���ʽ��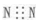 | |
| B�� | ������Ϊ53��������Ϊ78�ĵ�ԭ�ӣ�${\;}_{53}^{131}$I | |
| C�� | S2-�Ľṹʾ��ͼ��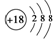 | |
| D�� | ��ϩ�ķ���ʽ��CH2=CH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
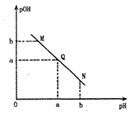 ij�¶��£���һ�����0.1mol•L-1�Ĵ�����Һ����μ��˵�Ũ�ȵ�NaOH��Һ����Һ�� pOH[pOH=-lgc��OH-��]�� pH �ı仯��ϵ�磬ͼ��ʾ��������
ij�¶��£���һ�����0.1mol•L-1�Ĵ�����Һ����μ��˵�Ũ�ȵ�NaOH��Һ����Һ�� pOH[pOH=-lgc��OH-��]�� pH �ı仯��ϵ�磬ͼ��ʾ��������| A�� | M����ʾ��Һ�ĵ�������ǿ��Q�� | |
| B�� | N ����ʾ��Һ�� c��CH3COO-����c��Na+�� | |
| C�� | Q������NaOH��Һ��������ڴ�����Һ����� | |
| D�� | M���N����ʾ��Һ��ˮ�ĵ���̶���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʼ˲��HCl��H2SO4��CH3COOH��Ӧ������� | |
| B�� | ����Ӧ����ʱCH3COOH�зų�H2��������� | |
| C�� | �ռ���ͬ�����H2��CH3COOH����ʱ��� | |
| D�� | ����Ӧ����ʱHCl��H2SO4�ռ���H2�������ͬ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com